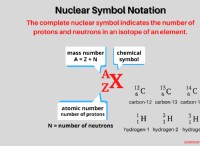
同位体の理解
* 同位体 同じ要素(同じ数の陽子)の原子ですが、中性子の数は異なります。これにより、異なる原子質量が生じます。
* 原子質量 元素のすべての自然に発生する同位体の質量の加重平均です。
亜鉛の同位体
亜鉛には、自然に発生する5つの同位体があります。
|同位体|存在量(%)|原子質量(AMU)|
| ---------------- | ------------------ | -----------------------------------------------------------------------------------------
| ⁶⁴Zn| 48.63 | 63.929142 |
| ⁶⁶Zn| 27.90 | 65.926037 |
| ⁶⁷Zn| 4.10 | 66.927131 |
| ⁶⁸Zn| 18.75 | 67.924848 |
| ⁷⁰Zn| 0.62 | 69.925325 |
原子質量の計算
1。各同位体の原子質量にその存在量(小数として表される)を掛けます。
*(63.929142 AMU * 0.4863) +(65.926037 AMU * 0.2790) +(66.927131 AMU * 0.0410) +(67.924848 AMU * 0.1875) +(69.925325 AMU * 0.0062)
2。結果を一緒に追加します。
この計算の結果は、亜鉛の原子質量になります。これは約 65.38 AMU です 。
注: 周期表の亜鉛の原子質量は、丸めまたはより正確な同位体データの使用により、この計算値からわずかに異なる場合があります。