* 分子間力の弱い: これらの物質の分子は、互いに弱い魅力を持っています。これらの力は、ロンドンの分散力、双極子型双極子相互作用、水素結合など、液体状態に分子をまとめる責任があります。これらの力が弱い場合、熱エネルギーによって簡単に克服でき、分子が気相に逃げることができます。
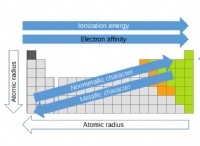
* 低分子量: 低分子量物質は分子間力が弱い傾向があり、ガスである可能性が高くなります。これは、重い分子にはより多くの電子があり、ロンドンの分散力が強くなるためです。
* 高蒸気圧: 沸点が低い物質は、室温で蒸気圧が高くなります。これは、かなりの数の分子がすでに気相にあることを意味し、液体からガスへの移行は容易に起こります。
簡単なアナロジーは次のとおりです。手を握っている人々のグループがあると想像してください。彼らがゆるく保持している場合、彼らは簡単にバラバラになり、自由に動くことができます。これは、分子間力が弱い物質のようなものです - 分子は簡単にガスになります。
例:
* ヘリウム(He): 分子間力が弱い非常に小さな原子であるため、あらゆる要素の中で最も低い沸点(-268.9°C)があります。
* 窒素(N2): 窒素分子間のロンドン分散力が比較的弱いため、-195.8°Cで沸騰します。
* メタン(CH4): -161.5°Cの沸点を持つ単純な炭化水素。分子間のロンドン分散力のみがあります。
対照的に、水(H2O)のような沸点が高い物質は、強い水素結合を持ち、室温で液体を作ります。