* 解決策: 塩を水に溶けると、均質混合物を形成します ソリューションと呼ばれます 。このソリューションはまだ液相にあります 。
* 飽和溶液: 水に塩を加え続けると、最終的には水が塩を溶かすことができなくなります。この点は、飽和点と呼ばれます 、および混合物は飽和溶液です 。まだ液相にあります 。
* サスペンション: 飽和点を超えてさらに多くの塩を追加すると、余分な塩は溶けず、不均一な混合物を形成します サスペンションと呼ばれます 。この懸濁液には、液相と固体の両方の相の両方があります 。
したがって、混合物の位相は次のとおりです。
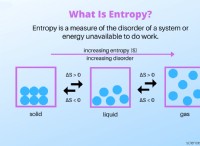
* 液体: 塩が水の中に完全に溶けるとき(溶液)
* 液体と固体: 塩が水の中に完全に溶けないとき(懸濁液)
混合物の位相は温度で変化する可能性があることを覚えておくことが重要です 。たとえば、塩と水の飽和溶液を加熱すると、より多くの塩を溶かすことができ、混合物は液相に残ります。