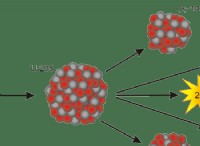
* プロトンは要素を定義します: 原子核内の陽子の数は、それがどの要素であるかを決定します。たとえば、すべての炭素原子には6つのプロトンがあります。
* 同位体は、同じ要素のバリエーションです: 同位体は、同じ数のプロトンを持っているが、異なる数の中性子を持つ同じ元素の原子です。これは、彼らが同じ原子数(陽子の数)を持っているが、質量数が異なることを意味します(陽子 +中性子)。
* 中性子は原子質量に影響します: 中性子は原子の質量に寄与します。同じ元素の異なる同位体は、異なる数の中性子を持っているため、異なる原子質量を持っています。
* 電子バランス陽子: 中性原子では、電子の数は常にプロトンの数に等しくなります。これにより、正と否定的な料金のバランスが保証されます。
例:
*炭素12には、6つのプロトン、6つの中性子、および6つの電子があります。
*炭素-14には、6つの陽子、8つの中性子、6つの電子があります。
どちらも6つのプロトンを持っているため、どちらも炭素原子ですが、中性子の数と原子質量が異なります。