* 反応性は相対的です: 反応性は、要素が反応しているものに依存します。たとえば、フッ素は全体的に最も反応性の高い非金属ですが、他の非金属とは異なる金属とは異なって反応します。
* 非金属対金属: 非金属と金属は非常に異なる方法で反応します。非金属はしばしば電子を獲得しますが、金属はそれらを失う傾向があります。
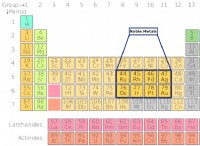
* グループ対期間: 周期表内では、反応性の傾向は一般にグループ(垂直列)と周期(水平行)で見られます。
ほとんどの反応群:
* グループ1(アルカリ金属): これらの金属は、1つの電子を失い、+1イオンを形成する傾向があるため、すべての金属の中で最も反応性があります。
* グループ17(ハロゲン): これらの非金属は、すべての非金属の中で最も反応性が高く、1つの電子を獲得して-1イオンを形成する傾向があります。フッ素は最も反応性の高いハロゲンです。
* グループ2(アルカリアース金属): これらの金属も非常に反応的ですが、2つの電子を失うため、アルカリ金属よりもそうではありません。
* グループ16(カルコジェン): このグループには、酸素や硫黄などの非常に反応性のない非金属が含まれています。
期間内の反応性:
* 期間にわたる: 一般に金属特性は減少しますが、非金属文字は一般に増加します。 これは、一定期間で最も反応性のない非金属が右側にあることを意味し、一定期間で最も反応性のある金属は左側にあります。
重要な注意: 反応性は、次のような要因によっても影響を受ける可能性があります。
* 原子サイズ: より小さな原子はより反応的になる傾向があります。
* 電気陰性度: 電気陰性度が高い(電子を引き付ける傾向)の元素はより反応的です。
* イオン化エネルギー: 低イオン化エネルギー(電子を除去するために必要なエネルギー)の要素はより反応的です。
要約: コンテキスト(反応物)を指定せずに、どの家族が「最も反応的」であるかを明確に言うことはできません。ただし、アルカリ金属は一般に最も反応性のある金属であり、ハロゲン(特にフッ素)は一般に最も反応性のない非金属です。