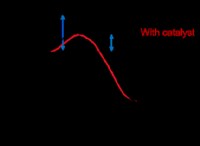
単一代表反応の理解
単一代替反応は、より反応性のある要素が化合物からそれほど反応性の低い要素を変位させると発生します。この一般的なパターンに従います。
* a + bc→ac + b
どこ:
* a より反応的な要素です。
* b より反応性の低い要素です。
* c 元素または多原子イオンです。
単一代替反応の可能性を決定する要因
1。アクティビティシリーズ(反応性シリーズ):
*最も重要な要因は、関係する要素の相対的な反応性です。
*アクティビティシリーズは、反応性の低下の順に要素をリストします。
*アクティビティシリーズの高金属は、化合物からシリーズの低い金属を置き換えます。
*たとえば、マグネシウム(Mg)は活性系列の銅(Cu)よりも高いため、マグネシウムは硫酸銅(Cuso₄)の溶液から銅を置き換えます。
2。金属と非金属:
*単一置換反応には、多くの場合、金属と非金属が含まれます。
*金属は一般に、化合物から別の金属を置き換えます。
*ハロゲン(非金属)は、化合物から別のハロゲンを置き換えることができます。
例
* 硫酸銅(II)と反応するマグネシウム:
* mg +cuso₄→mgso₄ + cu
*マグネシウムは銅よりも反応性が高いため、化合物から銅を置きます。
* 臭化カリウムと反応する塩素:
* cl₂ + 2kbr→2kcl +br₂
*塩素は臭素よりも反応性が高いため、化合物から臭素を変位させます。
反応が発生するかどうかを予測する方法
1。反応物と生成物を識別します: 関係する要素と化合物を決定します。
2。アクティビティシリーズを参照してください: 関係する要素の反応性を比較します。
3。ルールを適用します: 変位しようとする要素が化合物の元素よりも反応性が高い場合、単一代替反応が発生する可能性があります。
注: すべての単一置換反応が自発的であるわけではありません。発生するために特定の条件(熱など)が必要になる場合があります。
分析したい特定の反応がある場合はお知らせください!