* いくつかの価電子電子: 通常、金属には 1、2、または3つの価電子があります 。これらは、原子の最も外側のエネルギーレベルの電子であり、結合に関与するものです。
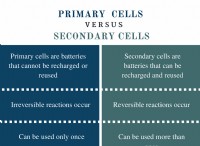
* 比較的簡単に負けます: 価電子電子がほとんどないため、金属は比較的簡単にそれらを失う傾向があり、積極的に帯電したイオン(陽イオン)になります。電子を失うことのこの容易さは、金属特性の重要な要素です。
* 導電率: 金属中の緩く結合された価電子電子は、材料全体を自由に移動し、優れた電気導電率と熱伝導率を可能にします。
ここに故障があります:
* グループ1(アルカリ金属): 1価電子
* グループ2(アルカリアース金属): 2価電子
* 遷移金属: さまざまな数の原子価電子ですが、通常は1または2です。
* 他の金属: 他のほとんどの金属には、3つ以下の原子価電子があります。
例外:
一般的な傾向は当てはまりますが、いくつかの例外があります。たとえば、水銀(HG)とスズ(SN)は、電子構成のために一意の動作を持っています。
金属の価電子の特定の側面についてもっと詳細をご希望の場合は、お知らせください!