酸と塩と水を生成するベースの間の反応。
その理由は次のとおりです。
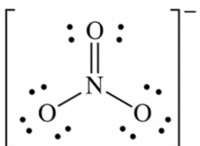
* 酸: 溶液中の水素イオン(H+)を放出する物質。
* ベース: 溶液中の水酸化物イオン(OH-)を放出する物質。
* 塩: 酸と塩基の反応から形成されたイオン化合物。
* 水: 塩基からの酸と水酸化物イオンの水素イオンの組み合わせによって形成されます。
例:
* 塩酸(HCl) +水酸化ナトリウム(NAOH) ->塩化ナトリウム(NaCl) +水(H2O)
この例では、HClは酸、NaOHはベース、NaClは塩、H2Oは水です。
重要な注意: 中和反応はしばしば熱の放出を伴うため、発熱反応になります。