pHと導電率は関連していますが、直接比例しません:
* pHは酸性度/アルカリ度を測定します: 低いpHは、水素イオン(H+)の濃度が高いことを示します。
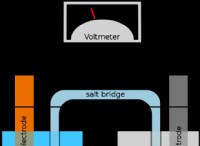
* 導電率は、電流を運ぶソリューションの能力を測定します: これは、荷電粒子(イオン)の存在に依存します。
接続方法:
* 酸と塩基は導電率に寄与する可能性があります: 強酸と塩基は完全にイオンに分離し、導電率が大幅に増加します。
* 他のイオンも重要です: 溶液の導電率は、pHからのイオンだけでなく、イオンの総濃度に依存します。 たとえば、高濃度の溶解塩を持つ溶液は、そのpHに関係なく伝導性があります。
例:
* 純水: イオン化が限られているため、導電率は非常に低い。
* 強酸溶液(例:HCl): H+濃度が高いということは、高い導電率を意味します。
* 強いベースソリューション(例:NAOH): 高OH濃度は高い導電率を意味します。
* 塩溶液(例:NaCl): pHに関係なく、Na+およびCl-イオンの存在による高い導電率。
要約:
酸性度が強酸によるものである場合、pHが低い場合は *時々 *導電率が高くなります。しかし、それは普遍的なルールではありません。導電率はイオンの総濃度に依存し、それはpH以外の因子に影響を与える可能性があります。