* 原子の反応性を決定します: 価電子の数と配置は、原子が他の原子とどのように相互作用するかを決定します。原子は、価電子電子を獲得、失い、または共有して安定した電子構成を実現する傾向があります。
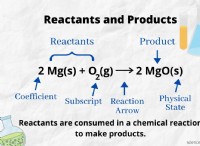
* 化学結合を形成します: 原子価電子は、化学結合の形成に直接関与しています。
* イオン結合: イオン結合を形成する原子価の電子を獲得または失う傾向が強い原子。 1つの原子は電子を失い、正に帯電したイオン(陽イオン)になり、もう1つの原子は電子を負に帯電したイオン(アニオン)にします。反対の料金はお互いを引き付けます。
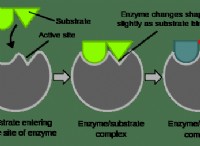
* 共有結合: 原子は価電子電子を共有して、安定した電子構成を実現します。この電子の共有は、共有結合の形成につながります。
* 金属結合: 金属では、原子価電子は非局在化し、構造全体を通して自由に移動し、金属原子を結合する「電子の海」を作成します。
* それらは化合物の特性に影響を与えます: 原子結合が一緒に結合する方法は、得られる化合物の物理的および化学的特性に直接影響します。たとえば、形成された結合のタイプは、融点、沸点、導電率、およびその他の特性を決定します。
要約: 価電子は、原子の最も外側の電子です。それらの挙動は、原子の反応性を支配し、それが他の原子とどのように結合するかを決定し、最終的に得られた化合物の特性に影響を与えます。それらは、分子と化合物を一緒に保持する「接着剤」です。