基本を理解する
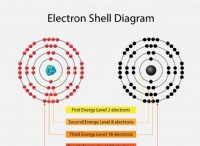
* 原子番号(z): これは、原子核内の陽子の数です。要素を定義します。 たとえば、すべての炭素原子の原子数は6です。
* 質量数(a): これは、原子核の陽子と中性子の総数です。
* 同位体: 同じ元素の原子(同じ原子数)が、中性子の数が異なる(したがって異なる質量数)。
原子質量と同位体の数を見つける
1。要素を識別します: 要素の名前またはシンボルは、原子番号を教えてくれます。
2。質量数を探してください: 質量数は通常、要素シンボルの前に上付き文字として書かれています。たとえば、炭素-14には質量数が14(¹⁴c)です。
3。中性子の数を計算します: 質量数から原子数(陽子の数)を減算します。たとえば、炭素-14には8つの中性子があります(14-6 =8)。
例:炭素-14
* 要素: 炭素(シンボル:c)
* 原子番号: 6(すべての炭素原子には6つのプロトンがあります)
* 質量数: 14
* 中性子の数: 14-6 =8
原子質量(平均原子質量)の発見
周期表にリストされている原子質量は、元素のすべての自然に発生する同位体の平均原子質量です。次の手順を使用して計算されます。
1。同位体とその存在量を識別します: 自然界の各同位体の相対的な存在量を知る必要があります。この情報は通常、テーブルに記載されています。
2。各同位体の質量にその存在量を掛けます: たとえば、炭素-12の豊富さは98.9%で、炭素-13の存在量が1.1%である場合、炭素12(12 AMU)の質量が0.989、炭素-13(13 AMU)の質量が0.011に増加します。
3。製品を一緒に追加: これにより、元素の平均原子質量が得られます。
キーポイント
* 原子番号は変更されません: 要素の原子番号は一定です。
* 同位体には、中性子の数が異なります: これは、異なる質量数につながります。
* 平均原子質量は加重平均です: それは、自然界の各同位体の相対的な存在量を反映しています。
他に質問があるか、その他の例が必要な場合はお知らせください!