1。 H2のグラムをH2:のモルに変換します
* H2:のモル質量 2.016 g/mol
* H2:のモル (1.57104 g H2) /(2.016 g / mol)=0.78 mol H2
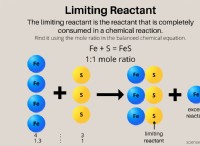
2。バランスのとれた化学式を使用して、モル比を見つけます:
反応のバランスの取れた化学式は次のとおりです。
N2 + 3H2→2NH3
*方程式から、3モルのH2が2モルのNH3を生成することがわかります。
3。生成されたNH3のモルを計算します:
* nh3のモル: (0.78 mol H2) *(2 mol nh3 / 3 mol H2)=0.52 mol nh3
4。 NH3のモルをNH3:の分子に変換します
* Avogadroの番号: 6.022 x 10^23分子/mol
* NH3の分子: (0.52 mol nh3) *(6.022 x 10^23分子/mol)= 3.13 x 10^23分子NH3
したがって、NH3の約3.13 x 10^23分子は1.57104 g H2から生成されます。