ゲイの法則によると、一定の体積に保たれた特定の質量の気体によって加えられるリュサックの圧力は、気体が一定の体積に保たれているとき (または一定の質量に保たれ、一定の体積に保たれると一定の体積に保たれる)。言い換えれば、ガスの質量が固定され、ガスの体積が一定である場合、ガスによって加えられる圧力はガスの温度に比例します。
1808 年、フランスの化学者ジョセフ ゲイ リュサックがこの法則を思いつき、彼の雑誌に掲載しました。ゲイの法則によれば、ルサックの次の数式は次のように記述できます。
P ∝ T; P/T =k
場所:
ガスによって加えられる圧力は、文字 P で表されます。
ガスの絶対温度は文字 T で表されます。
k は定数です。
一定の体積のガスの圧力と絶対温度の関係をグラフで表したもの。
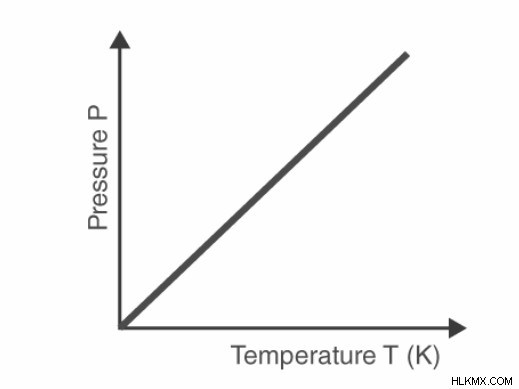
グラフに基づいて、ガスが最終的に凝縮して液体になるまで、(一定の体積に維持されている) ガスの圧力は、冷却されるにつれて継続的に低下すると推測できます。
式と導出
初期圧力と温度および最終圧力と温度の間の関係により、ゲイの法則リュサックは、初期圧力と温度の比率が、次の気体の最終圧力と温度の比率に等しいことを意味します。一定の体積に保たれた固定質量。以下は、この数式の式です:
(P1/T1) =(P2/T2)
場所:
初期圧力は P1 で示されます。
T1 は、実験が開始された温度です。
最終圧力は P2 で示されます。
最終温度は T2 で示されます。
気体に関して言えば、この式は圧力と温度の比例関係から導き出すことができます。 P ∝ T は、質量が固定されているが体積が一定の気体の場合、以下が成り立ちます:
P1/T1 =k のとき、初期圧力/初期温度が両方とも一定であることを意味します。
最終圧力/最終温度は k に等しい (最終圧力/最終温度は定数に等しい).
結果として、P1/T1 =P2=/T2 =k.
代わりに、P1T2 =P2T1.
同性愛者のルサック夫妻を次の例で説明します:
加圧されたエアゾール容器 (消臭剤の缶やスプレー塗料の缶など) が加熱されると、ガスによる圧力が上昇して爆発が発生する可能性があります。コンテナ(ゲイ法による)。このため、多くの加圧容器には、容器を火気から遠ざけ、涼しい環境で保管する必要があることを示す警告ラベルが貼られています。

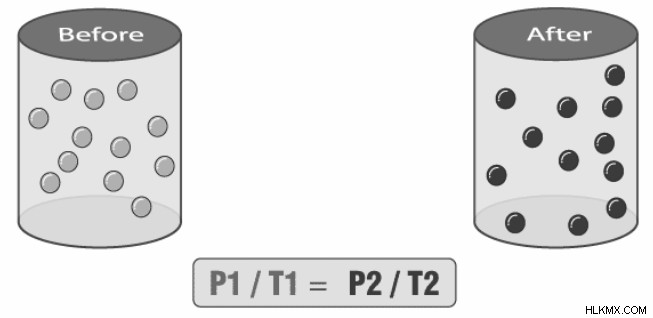
このセクションには、ガスの体積が一定値に維持されている間にガスの絶対温度が上昇したときに発生する圧力の増加を説明する図が含まれています。圧力鍋を使用する場合、ゲイ法ルサックの別のアプリケーションを観察できます。加熱によって容器内の蒸気の圧力が高まると、容器内の圧力が上昇します。容器内の温度と圧力が高いため、食品は通常よりも早く調理されます。
結論
気体の体積が一定に保たれている場合、Gay-law Lussac は、与えられた気体の質量の圧力は気体の絶対温度によって直接変化し、その逆も成り立つと述べています。これは、理想気体の法則の特定のアプリケーションです。封入されたガスの圧力がその温度に正比例することを確立し、彼が最初に定式化した圧力の法則で知られるゲイ-リュサックは、圧力の法則を発見したとされています。また、彼は、一定の体積に維持された一定質量の気体の圧力と温度の関係を示す説得力のある証拠を最初に発表したとされることもあります.