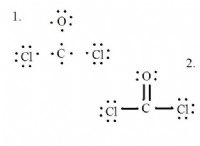化学結合にはさまざまな種類がありますが、最も一般的なのは次のとおりです。
* イオン結合: これらの結合は、電気陰性度(電子を引き付ける能力)に大きな違いがある原子間に形成されます。 1つの原子は電子を失い、積極的に帯電したイオン(陽イオン)になり、もう1つの原子は電子を獲得して負に帯電したイオン(アニオン)になります。反対の電荷が互いに引き付けられ、イオンを結晶格子にまとめます。
* 共有結合: これらの結合は、電子を共有する原子間に形成されます。共有電子は両方の原子の核に引き付けられ、強い結合が生じます。共有結合は、共有されている電子のペア数に応じて、単一、二重、またはトリプルにすることができます。
* 金属結合: これらの結合は金属原子間で発生します。金属原子の価電子は非局在化されており、金属格子全体で自由に移動できます。これにより、強い結合が生まれ、導電率や順応性などの金属の特性を説明します。
したがって、それは単なる力ではなく、原子を一緒に保持して化合物を形成する力の組み合わせです。特定のタイプの結合は、関連する要素とその特性によって異なります。