浸透と拡散は、物質輸送の 2 つの重要なタイプです。ここでは、浸透と拡散の定義、各プロセスの例、およびそれらの違いについて説明します。
浸透と拡散の定義
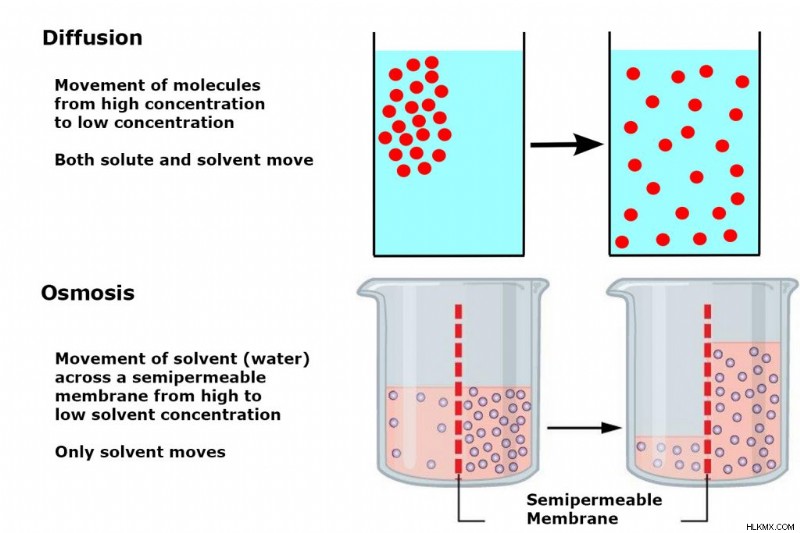
浸透 – 浸透とは、希釈溶液から濃縮溶液への半透膜を横切る溶媒粒子 (通常は水) の移動です。溶媒は、濃度が膜の両側で均等になるまで、濃縮溶液を希釈します。
拡散 – 拡散とは、濃度の高い領域から濃度の低い領域への溶媒および溶質粒子の移動です。平衡状態では、正味の効果は媒体全体で均一な濃度になります。
浸透と拡散の例
浸透の例 :グミベアキャンディーを浸すことは、浸透の簡単なデモンストレーションです。キャンディーのゼラチンは半透膜として機能します。生物学の良い例は、真水に入れられたときの赤血球の膨張と、塩水に入れられたときの収縮 (クレネーション) です。水を吸収する植物の根毛は、浸透のもう 1 つの例です。
拡散の例 :拡散の良い例は、香水が部屋全体を満たす方法です。別の例は、細胞膜を通過する小分子とイオンの移動です。食品着色料を水に落とすことは、拡散の一例です。他のプロセスが発生しますが、拡散が主な輸送方法です。
類似点の比較
浸透と拡散には類似点があります:
- 浸透と拡散はどちらも受動的な輸送プロセスです。言い換えれば、それらは自然発生的であり、発生するのに必要なエネルギーはありません.
- 両方のプロセスで溶液の濃度が均一になります。
浸透と拡散
浸透と拡散には主な違いがあります:
- 浸透は半透膜を介してのみ発生しますが、拡散は任意の混合物で発生する可能性があります (半透膜を介したものを含む)。
- 生物学では、浸透は水の動きのみを指します。化学では、水以外の溶媒が移動することがあります。拡散は、両方の分野で同じ意味を持ちます。
- 浸透では、溶媒のみが膜を自由に移動できます。拡散では、溶媒粒子と溶質粒子の両方が自由に動きます。
キー ポイント

- 浸透と拡散はどちらも、濃度を均一化する受動的な輸送プロセスです。言い換えれば、それらが発生するためにシステムにエネルギーを供給する必要はありません。
- 拡散では、粒子は平衡に達するまで高濃度から低濃度に移動します。
- 浸透には、溶媒粒子のみを移動させる半透膜があります。溶媒 (通常は水) は、平衡に達するまで移動します。
- 浸透圧に惑わされないでください。バリアの両側の濃度を均等にする唯一の方法は、水を移動させることです。溶媒分子は低い溶媒濃度から高い溶媒濃度に移動しますが、高い溶質濃度から低い溶質濃度に移動します。溶液の濃度が重要です。
- 浸透は、溶媒のみが移動する半透膜を含む拡散の特殊なケースと見なすことができます。
| 拡散 | 浸透 |
|---|---|
| 溶媒と溶質は、エネルギーまたは濃度が最も高い領域から、エネルギーまたは濃度が最も低い領域に移動します。 | 高エネルギーまたは高濃度の領域から低エネルギーまたは低濃度の領域に移動するのは、水またはその他の溶媒のみです。 |
| 拡散は、液体、固体、気体など、あらゆる媒体で発生する可能性があります。 | 浸透は液体媒体でのみ発生します。 |
| 拡散には半透膜は必要ありません。 | 浸透には半透膜が必要です。 |
| 拡散した分子の濃度が等しくなり、使用可能なスペースが満たされます。 | メンブレンの両側で溶媒の濃度が等しくならない |
| 通常、静水圧と膨圧は拡散には適用されません。 | 静水圧と膨圧は浸透に対抗します。 |
| 拡散は、溶質ポテンシャル、圧力ポテンシャル、または水ポテンシャルに依存しません。 | 浸透は溶質のポテンシャルに依存します。 |
| 拡散は主に他の粒子の存在に依存します。 | 浸透は主に、溶媒に溶解した溶質粒子の数に依存します。 |
| 拡散は受動的なプロセスです。 | 浸透は受動的なプロセスです。 |
| 拡散の動きは、システム全体の濃度 (エネルギー) を均等にすることです。 | 浸透の動きは、溶媒濃度を均一化しようとしますが、これは達成されません. |
その他の種類の輸送プロセス
拡散にはさまざまな種類があります。浸透と対比される拡散のタイプは単純拡散です。能動拡散と促進輸送は、他の物質輸送プロセスです。
- 単純拡散 – 濃度が均一になるまで、粒子は高濃度から低濃度に移動します。
- 能動輸送 – 溶質粒子は低濃度から高濃度に移動します。生物学では、酵素 (タンパク質) が膜を越えて溶質を運び、エネルギー (ATP) が必要です。
- 便利な交通手段 – 溶質は、膜貫通タンパク質の助けを借りて、膜を横切って高濃度から低濃度に移動します。これは、大きな分子が半透膜を通過する方法です。これは単純な拡散のような受動的な輸送プロセスです。
浸透にもさまざまな種類があり、すべて半透膜が関与しています:
- 定期浸透 – 溶媒粒子は、平衡に達するまで高濃度から低濃度 (溶質濃度の低濃度から高濃度) に移動します。
- 逆浸透 (RO ) – 溶質と水の溶液では、水圧によって水が半透膜を通過します。その結果、膜の片側の溶質濃度が増加し、反対側に精製水が追加されます。溶媒は濃度勾配に逆らって移動するため、エネルギー (圧力) が必要です。
- 正浸透 (FO) – 浸透圧により、半透膜を横切って水が引き寄せられ、溶質から分離されます。逆浸透と正浸透はどちらもエネルギー (圧力) を必要としますが、逆浸透は水を押し出し、正浸透は水を引き寄せる、または「引き寄せ」ます。また、逆浸透は新鮮な飲料水を生成できますが、正浸透の生成物には溶質粒子が含まれます。たとえば、砂糖と塩を使用して不純な水から水を抽出し、非常用飲料を作ることができます。
拡散と胸水
エフュージョンは、気体に見られる一種の物質輸送プロセスです。拡散により、ガス粒子は容器を通して自由に分散できます。エフュージョンとは、平均自由行程 (粒子衝突間の距離) よりも小さい細孔を通るガス分子の輸送です。浸出は、拡散よりもゆっくりと発生します。流出速度は、グラハムの法則に従って、粒子の質量の平方根に反比例します。
参考文献
- Glater, J. (1998)。 「逆浸透膜開発の初期の歴史」 淡水化 . 117 (1–3):297–309. doi:10.1016/S0011-9164(98)00122-2
- ヘイニー、ドナルド T. (2001). 生物学的熱力学 .ケンブリッジ:ケンブリッジ大学出版局。 pp.130–136。 ISBN 978-0-521-79549-4.
- クレイマー、エリック;デビッド・マイヤーズ (2012)。 「浸透についてよくある5つの誤解」 American Journal of Physics . 80 (694):694–699. doi:10.1119/1.4722325
- Landau, L.D.; Lifshitz、E.M. (1980)。 統計物理学 (第3版)。巻。 5.バターワース・ハイネマン。 ISBN 978-0-7506-3372-7.
- ミューア、D. C. F. (1966). 「肺の気道におけるバルクフローと拡散。」 British Journal of Diseases of the Chest . 60 (4):169–176. doi:10.1016/S0007-0971(66)80044-X