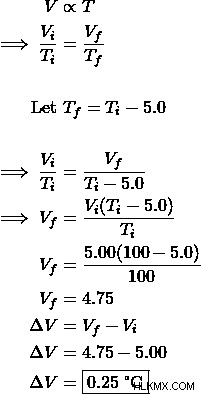シャルルの法則のコア コンセプト
この記事では、温度が体積にどのように関係するか、およびシステムの温度と体積の変化に関する問題を解決するためにシャルルの法則の公式を使用する方法を学びます。
他の記事で取り上げるトピック
- プレッシャーとは
- ダルトンの分圧の法則
- アボガドロの法則
- ボイルの法則
- 混合ガス法
- 理想気体の法則
- ファン デル ワールスの状態方程式
- 運動分子理論
- ヘンリーの法則
考慮すべき重要事項
この記事で説明する気体の法則は、理想気体にのみ適用されます。これについては、The Ideal Gas Law の記事で読むことができます。 .
体温を上げる
1 リットルのガスが入ったピストンを考えてみましょう。ピストンは自由に容積を変更できるため、圧力は一定に保たれます。
ここで、気体の温度を上げるとどうなるかを考えてみましょう。運動分子理論から、ガスのサンプルの温度がその速度に直接関係していることがわかっています。
プレッシャーに関する記事から、プレッシャーとは 、ガスの圧力は、壁に衝突するときに加えられる力の結果であることを知っています。この力は、圧力に関する記事に記載されているように、次の式で計算できます。 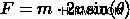 .
.
温度が上昇するにつれて、  が増加するため、力が増加します。ただし、ピストンは自由に容積を変えることができるため、圧力は一定のままです。ボイルの法則から、圧力は体積に反比例することがわかっているため、ピストンは温度の変化を考慮して体積を増やします。
が増加するため、力が増加します。ただし、ピストンは自由に容積を変えることができるため、圧力は一定のままです。ボイルの法則から、圧力は体積に反比例することがわかっているため、ピストンは温度の変化を考慮して体積を増やします。
シャルルの法則
フランスの物理学者ジャック・シャルルもこの現象に気づき、温度と体積の関係を発見しました。これは、シャルルの法則またはシャルルの法則式として知られているもので、次のように書くことができます。 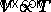 .次のように表現することもできます。
.次のように表現することもできます。 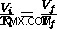 、変数がマークされている場所
、変数がマークされている場所 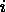 は初期条件、およびマークされた変数
は初期条件、およびマークされた変数 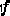 が最終版です。
が最終版です。
アプリケーション
この比例関係により、シャルルの法則を使用して、システムが温度の変化にどのように反応するか、またはシステムが体積の変化にどのように反応するかを確認できます (両方とも圧力が一定の場合)。温度が上昇すると体積が増加し、その逆も同様です。
シャルルの法則の例の問題
例のチャールズの法則の問題を解く方法は次のとおりです。
問題:21 °C の酸素ガスの 2.00 L ピストンを 1.00 L に圧縮したときの温度変化を計算します。
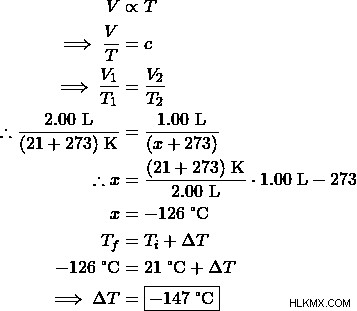
これは別のチャールズの法則の問題です。
問題:5.00 L の酸素を 100 °C から 5.0 °C 冷却すると、体積はどのように変化しますか?