コア コンセプト
アルケン 有機化学および生化学において最も一般的で重要な分子の 1 つです。この記事では、アルケンの構造、その命名法、およびその反応のいくつかを学びます.
他の記事で取り上げるトピック
- アルキンとは?
- 構造異性体
- 幾何異性
- E1 反応
- E2 反応
アルケン構造
アルケンは、炭素-炭素二重結合 (C=C、一方の結合がシグマ結合、もう一方の結合がパイ結合) を含む炭化水素 (完全に炭素と水素からなる化合物) です。炭素-炭素二重結合は、アルケンの官能基です。
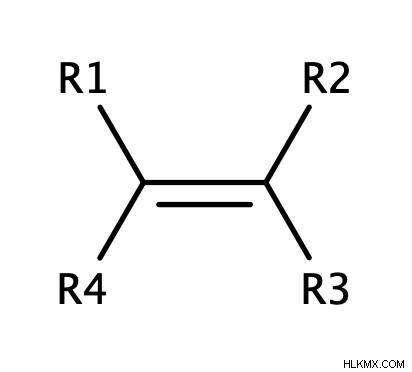

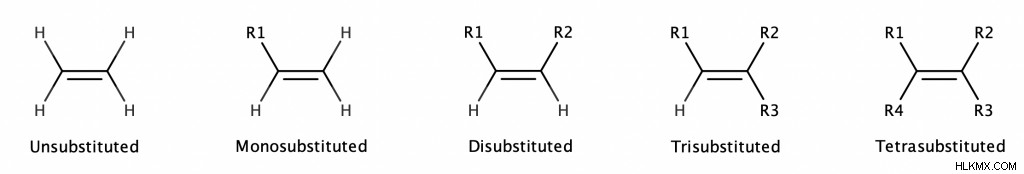
アルケンは、C=C 結合の各末端の水素原子がアルキル (またはハロゲン化アルキル) 基で置換されている場合、置換されていると言われます。
アルケンの概要
- 構造:別の炭素に二重結合した炭素。

- 一般式:Cn H2n 、ここで n ≥ 2
- 酸性度:アルカンより酸性
- 溶解度:水には不溶ですが、ジエチル エーテルなどの非極性有機溶媒には溶けます
- C=C 結合長:1.33 Å
- C=C 結合強度:636 kJ mol
- IR 分光法:Csp を持つアルケン –H 結合 (つまり、四置換されていないアルケン) は 3100 cm にピークがあります
アルケンの立体化学
この概念については、構造異性体、幾何異性、シス トランス異性体、立体異性体、およびキラル中心という記事で広く取り上げています。
したがって、以下の情報は簡単な復習になります。
二重結合の剛性 (回転できない) により、置換アルケン (つまり、C=C 結合の各末端の水素原子が水素以外の置換基に置き換えられているアルケン) は、一対の立体異性体として存在できます。化学者は、シス/トランスまたは E/Z 用語を使用して、これらの立体異性体を記述します。
シス/トランス
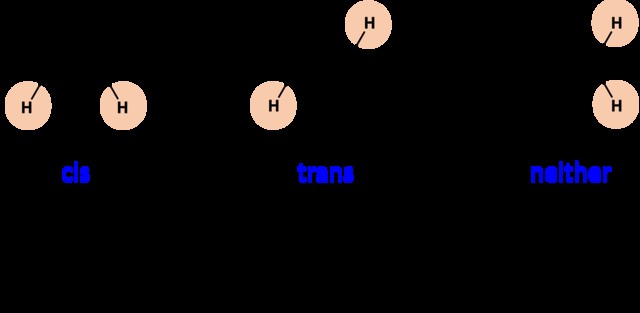
化学者は、置換基が C=C 結合の異なる末端に接続されている二置換アルケンに cis/trans 用語を使用します。
- シス異性体は、二重結合の同じ側に同じ基を持っています。
- トランス異性体は、二重結合の反対側に同じ基を持っています。
東/西
化学者は、三置換または四置換アルケンに E/Z 用語を使用します。
E/Z 用語を使用するには、まず Cahn-Ingold-Prelog 規則を使用して置換基に優先順位を割り当てます (置換基の元素の原子番号が大きいほど、優先順位が高くなります)。次に、C=C 結合の両端に注意を向け、そこにある置換基のペアの優先度を比較します。
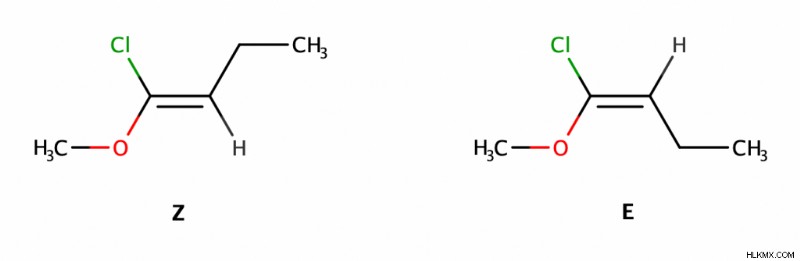
- E 異性体は、二重結合の反対側に優先順位の高い置換基を持っています。
- Z 異性体は、二重結合の同じ側に優先順位の高い置換基を持っています。
アルケン命名法
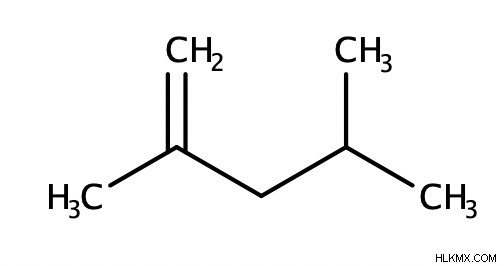
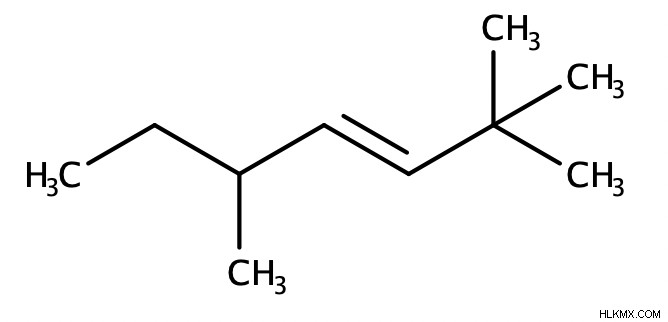
アルケン (他の官能基を含まない純粋なアルケン) に名前を付けるには、まず、C=C 二重結合を含む最長の鎖である親を特定します。次に、分子内の位置を示すために、二重結合と他の置換基 (存在する場合) に番号を割り当てます。二重結合には可能な限り小さい数を割り当てる必要があります。最後に、分子名の末尾に接尾辞「ene」を付けます。必要に応じて、分子名の前に「cis」、「trans」、「E」、または「Z」を付けなければなりません。
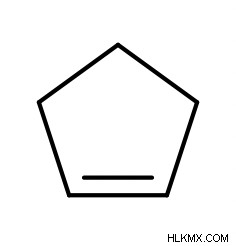
さらに、アルケンが環状分子の形をとる場合、親鎖の前に「シクロ」を置きます。
IUPAC はまた、一般的なアルケンのいくつかの一般名を認識しています:エチレン、プロピレン、スチレンなど。
アルケンが分子の単なる置換基である場合 (つまり、より優先度の高い官能基が存在する場合)、親鎖と官能基の間に「en」を挿入します。また、位置を示すために「en」の前に数字を付けることを忘れないでください (この場合のみ二重結合は可能な限り低い数字にはなりません)。
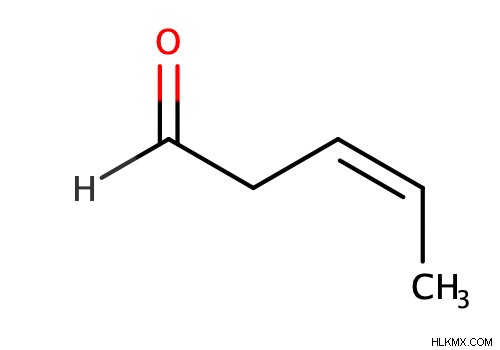
アルケン反応
一般的な反応の傾向
化学者は、他の複雑な分子を合成するための構成要素としてアルケンをよく使用します。これは、アルケンが付加反応を起こしやすいためです。アルケンの C=C 二重結合は電子が豊富であるため、塩基または求核試薬として機能します。
脱離反応
化学者は脱離反応を利用してアルケンを形成します。除去反応については、E2 反応、E1 反応、E1 と E2 反応の理解の記事で詳しく説明しています。
E2 反応
E2 反応では、ルイス塩基がベータ水素をつかみ、脱離基が同時に離れます。これにより、一時的に負に帯電した炭素がその電子を一時的なカルボカチオンと共有して二重結合を形成します。
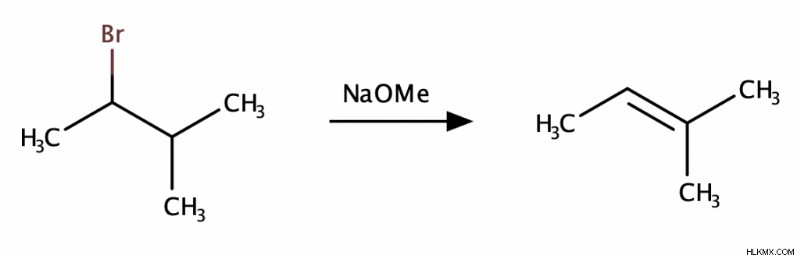
E1 反応
E1反応はE2反応と似ています。主な違いは、E1 反応では脱離基が最初に脱離し、カルボカチオンを形成することです。その後、基地がやって来て、ベータ水素をつかみます.
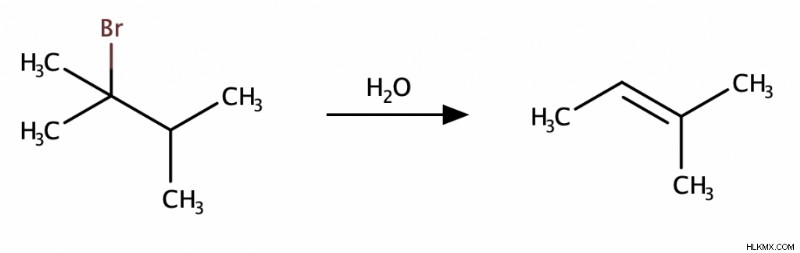
付加反応
立体化学と位置化学
アルケンの付加反応を見る前に、化学者が反応の立体化学と位置化学を説明するために使用する用語に慣れることをお勧めします。
- 立体化学:シン付加、アンチ付加
- 位置化学:マルコフニコフ付加と反マルコフニコフ付加
アルケンの水素化
アルケンの水素化では、2 つの水素 (H) 原子が、Pt、Pd、または Ni などの金属触媒の助けを借りて、C=C 二重結合を横切って追加されます。このリアクションはsynです 追加。
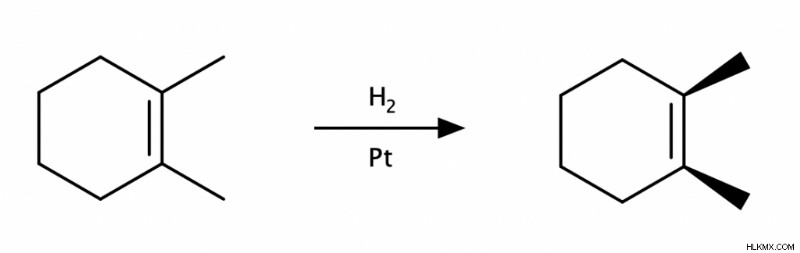
アルケンのハロゲン化水素化
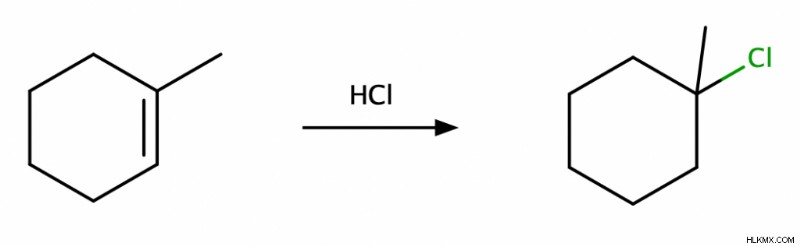
アルケンのハロゲン化水素化では、1 つの H 原子と 1 つのハロゲン原子が C=C 二重結合に付加されます。この反応はマルコフニコフです さらに、syn の混合物が得られます そしてアンチ
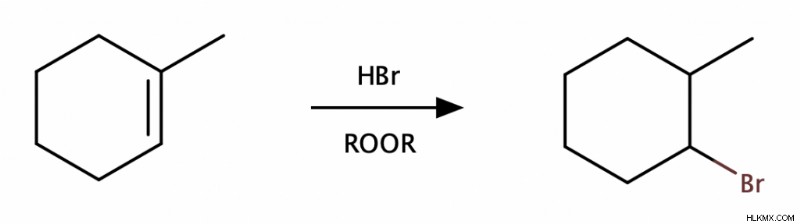
しかし、過酸化物 (ROOR) の存在下で HBr をアルケンに付加すると、奇妙なことが起こります。製品はまだ syn の混合物です そしてアンチ 、しかし反応は反マルコフニコフになります さらに、Br は置換度の低い炭素に行き着きます。
アルケンの水和
アルケンの水和では、1 つの H 原子と 1 つの OH 分子が C=C 二重結合に付加されます。この反応は、当社の試薬に応じて、マルコフニコフ反応または抗マルコフニコフ反応になります。
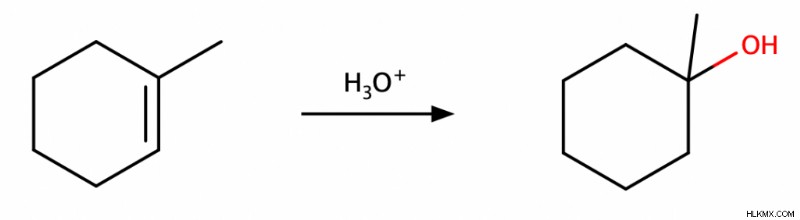
酸触媒ハイドレーション
その名前が示すように、この反応は、酸の存在下でアルケンに水を加えることを含みます。このリアクションは マルコフニコフ です syn の両方を与える そしてアンチ
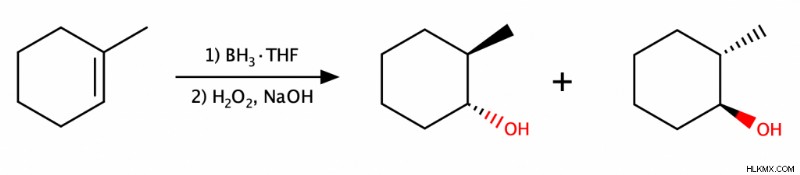
ハイドロボレーション - 酸化
この水和反応には 2 つのステップが含まれます。最初のステップであるハイドロボレーションでは、ボラン (BH3 ) アルケンにテトラヒドロフラン (THF) のような安定化溶媒。 2 番目のステップである酸化では、過酸化水素 (H2 O2 ) および水または NaOH のような水酸化物 (OH) ソース。この反応は反マルコフニコフです syn のみを与える
アルケンのジヒドロキシル化
アルケンのジヒドロキシル化では、2 つの OH 分子が C=C 二重結合に付加され、アルケンが効果的にジオールに変わります。両方の炭素に同じもの (つまり OH) を追加しているので、位置化学は関係ありません。対照的に、立体化学は非常に興味深いトピックです。反応は、当社の試薬に応じて、syn または anti になります。
抗ジヒドロキシル化
アンチを達成するには アルケンのジヒドロキシル化では、化学者はそのアルケンを最初にペルオキシ酸 (MCPBA など) で処理し、次に酸触媒条件下で水で処理します。過酸はアルケンをエポキシドに変え、水はエポキシドを開きます.
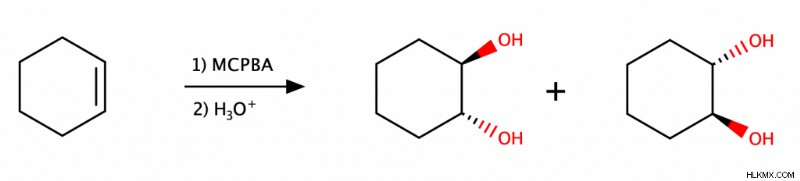
シンジヒドロキシル化
シンクロを達成するには アルケンのジヒドロキシル化、化学者は最初にそのアルケンを四酸化オスミウム (OsO4 )、次に硫化ナトリウム水溶液 (Na2 SO3 ) または水性水硫化ナトリウム (NaHSO3 ).
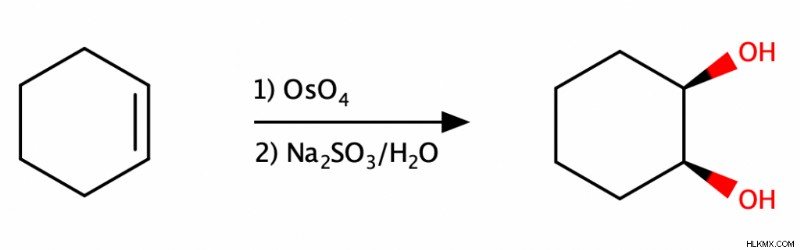
別の方法は、アルケンを冷過マンガン酸カリウム (KMnO4) で処理することです。 )および水酸化物源。
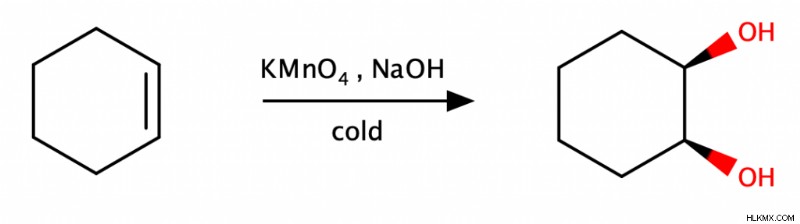
オゾン分解
オゾン分解は、化学者が C=C 結合を切断するために使用する多くの反応の 1 つです。オゾン分解を行うために、化学者は最初にアルケン溶液にオゾンを吹き込み、次にジメチルスルフィド (DMS) のような還元剤を溶液に加えます。その結果、C=C 結合が 2 つの C=O 結合に分割されます。
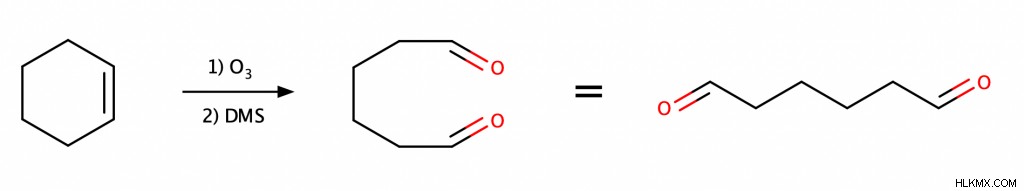
参考文献
- アミノ官能基
- カルボニル官能基
- カルボン酸官能基
- ケトエノール互変異性化
- アルドール縮合反応
- ディールス・アルダー反応