ヨウ素は、非金属の濃い灰色/紫黒色の光沢のある固体元素です。それは最も電気陽性のハロゲンであり、ハロゲンの中で最も反応性が低く、それでも多くの元素と化合物を形成することができます.
化学元素のヨウ素には記号「I」があります 原子番号は 53 です。ヨウ素は、安定したハロゲンの中で最も重いものです。ヨウ素は、STP で半光沢のある非金属の固体の形で存在し、摂氏 114 度の高温で溶けて濃い紫色の液体を形成します。摂氏 184 度で、ヨウ素は紫色のガスに沸騰します。その名前は古代ギリシャ語に由来し、「紫色」を意味します。
| グループ | グループ 17 (ハロゲン) |
| ピリオド | ピリオド5 |
| ブロック | pブロック |
| 電子配置 | [Kr] 4d10 5s2 5p5 |
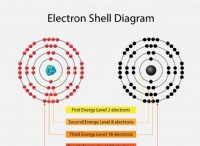
| シェルあたりの電子 | 2, 8, 18, 18, 7 |
| 酸化状態 | −1、+1、+3、+4、+5、+6、+7 (強酸性酸化物) |
上の表に見られるように、ヨウ素は、ヨウ化物 (I–)、ヨウ素酸 IO3– およびその他のさまざまな陰イオンを含む多くの酸化状態で発生します。ヨウ素はハロゲンの中で最も豊富で、最も豊富な元素の 61 番目の位置にあります。ヨウ素はまた、植物に見られる最も重い必須ミネラル栄養素です.
ヒトでは、甲状腺ホルモンの合成に不可欠です。ヨウ素の欠乏は、世界のほぼ 20 億人に深刻な影響を与えています。ヨウ素欠乏症は、知的障害と精神遅滞の世界で最も重要な予防可能な原因の 1 つです。
ただし、ヨウ素は非常に反応性が高く、他のハロゲンよりも反応性が低くなります.
ヨウ素の反応
ヨウ素と塩基の反応
ヨウ素 I2 は熱アルカリ水溶液と反応し、ヨウ素酸 IO3– を形成します。
3 I2(s) + 6 OH–(aq) IO3–(aq) + 5 I–(aq) + 3 H2O(l)
ヨウ素と酸の反応
金属のヨウ素化は、塩素化または臭素化よりも低い酸化状態を示します。ヨウ素分子 I2 は CCl4 と脂肪族炭化水素に溶解し、明るい紫色の溶液になります。
次の式では、ヨウ素 I2 が濃硝酸と反応してヨウ素酸が生成されます。
I2(s) + 10 HNO3(aq) 2 HIO3(s) + 10 NO2(g) + 4 H2O(g)
ヨウ素とハロゲンの反応
ヨウ素 I2 は室温でフッ素 F2 と反応し、フッ化ヨウ素 (V) を形成します。 250 °C の高温では、生成物はフッ化ヨウ素 (VII) です。 -45 °C の低温で、CFCl3 に懸濁すると、フッ化ヨウ素 (III) が形成されます。
I2(s) + 5 F2(g) ⟶ 2 IF5(l) [無色]
I2(g) + 7 F2(g) ⟶ 2 IF7(g) [無色]
I2(s) + 3 F2(g) ⟶ 2 IF3(s) [黄]
ヨウ素 (I2) は臭素 (Br2) と反応し、非常に不安定で低融点の固体臭化ヨウ素 (I) を形成します。
I2(s) + Br2(l) ⟶ 2 IBr(s)
ヨウ素 (I2) が過剰な塩素 (Cl2) と -80 °C で反応すると、塩化ヨウ素 (III) が形成されます。水の存在下では、ヨウ素酸が室温で形成されます。
I2(s) + 3 Cl2(l) ⟶ I2Cl6(s) [黄色]
I2(aq) + 6 H2O(l) + 5 Cl2(g) ⟶ 2 HIO3(aq) + 10 HCl(g)
ヨウ素と空気の反応
ヨウ素 I2 は、塩素や臭素と同様に、酸素 O2 や窒素 N2 と反応しません。
ただし、オゾン O3 と反応して、黄色の不安定な化合物 I4O9 を生成します。
ヨウ素と水との反応
ヨウ素 I2 は水と反応し、次亜ヨウ素酸塩の化合物 IO– を形成します。
I2(aq) + H2O(l) ⟶ IO– + 2 H+(aq) + I–(aq)
ヨウ素と金属/金属イオンとの反応
固体カドミウム、Cd は水相内では反応しませんが。ただし、気相では、Cd と I2 が反応し、CdI2(g) が形成されます。
スチール製の爆弾の製造では、高温高圧で、Cd と I2 に相当する量が反応して CdI を形成します。
Cd(s) + I2(aq) ⟶ Cd2+(aq) + 2 I–(aq)
Cd(g) + I2(g) ⟶ CdI2(g)
2 Cd(g) + I2(g) ⟶ 2 CdI(g)
I2 の形成下で、酸化状態が 2 を超えるマンガンは、酸性条件下で I– によって Mn(II) に還元されます。
MnO2(s) + 2 I–(aq) + 4 H+(aq) ⟶ Mn2+(aq) + I2(aq) + 2 H2O(l)
モリブデン (IV) 酸化物のような元素は、230 °C でヨウ化アルミニウム (III) と反応してヨウ化モリブデン (II) を生成します。
ハロゲン交換は、塩化タンタル (V) と過剰のヨウ化アルミニウム (III) との 400 °C での反応中に起こり、その結果、ヨウ化タンタル (V) が生成されます。
ヨウ素と水素の反応
ヨウ素の最も単純な化合物はヨウ化水素 (HI) であり、酸素と反応して水とヨウ素の組み合わせを生成する無色のガスです。
水素はI2と反応してヨウ化水素を形成します。室温では反応速度が遅く、温度を上げると反応速度が速くなります。
2 I2 + N2H4 H2O ⟶ 4 HI + N2
酸化ヨウ素とオキソ酸
4 つのオキソ酸:次亜ヨウ素酸 (HIO)、ヨウ素酸 (HIO3)、ヨウ素酸 (HIO3)、過ヨウ素酸 (HIO4 または H5IO6) は非常に重要です。
ヨウ素は水溶液中で溶解し、次の反応を形成します。
I2 + H2O ⇌ HIO + H+ + I–;Kac =2.0 × 10-13 mol2 l-2
I2 + 2 OH– ⇌ IO– + H2O + I–;Kalk =30 mol-1 l
次亜ヨウ素酸は不均化に対して不安定です。このようにして形成された次亜ヨウ素イオンは、すぐに不均化してヨウ化物とヨウ素酸塩になります:
3 IO– ⇌ 2 I– + IO– 3K =1020
さらに安定性が低いのは、ヨウ素酸 (HIO2) とヨウ素です。それらは、ヨウ化物からヨウ素酸塩への酸化の中間体としてのみ存在します。
結論
ヨウ素との反応から形成されるすべての化合物は非常に重要です。ヨウ素は塩に含まれており、人間が生きていく上で本質的に重要であると聞いたことがあるでしょう.ヨウ素は、一部の岩石、海水、および堆積物に自然に存在します。洗浄用消毒剤として水を浄化するために広く使用されており、スキンソープに使用されています。自然界に存在する放射性ヨウ素のほとんどは人工物です。ヨウ素は病気の治療にも使用され、医療検査にも使用されます.