周期表のグループ 2 には、6 つの要素があります。自然界に存在する酸化物はアルカリ性または塩基性であるため、そのように名付けられました。熱や火などの燃焼剤の影響を受けません。それらは非常に反応性が高く、自由な状態では地殻には存在しません。むしろ、ケイ酸塩、炭酸塩などのように結合した状態で見られます。
地球での出来事
- ベリリウム → ケイ酸塩鉱物に少量含まれています。
- マグネシウム → 炭酸塩、ケイ酸塩、ケイ酸塩として豊富に含まれています。地球上で 6 番目に多い元素です。
- カルシウム → 地殻に含まれる元素の中で 5 番目に多い。石灰岩、チョーク、大理石に炭酸カルシウムの形で含まれています。他の例には、石膏、蛍石などがあります。
- ストロンチウム → ストロンチアナイト (SrCO3) またはセレスタイト (SrSO4) の形で採掘されます。
- バリウム → バライトの形で採掘されます。
- ラジウム → は放射性元素です。ウラン、トリウム、アクチニウムの崩壊状態の形で発見されています。
物理的特性
-
結合の電子配置と性質:
(希ガス) ns2 は一般的な電子配置です。これらの元素の原子には、塗りつぶされた s サブシェルがあります。
-
イオン半径と原子半径:
イオン半径と原子半径は、周期表のグループを下るにつれて増加し続けます。それらは、s サブシェルからすべての電子を失い、サイズが中性原子よりも小さくなる可能性があります。それでも、彼らはまだグループを下っていきます.
-
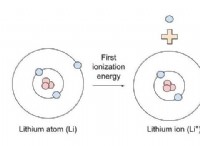
イオン化および水和エネルギー/エンタルピー:
それらは低いイオン化エンタルピーを持っていますが、次の理由により、周期表のグループ 1 元素のイオン化エンタルピーよりも大きくなっています:
- 核電荷が高く、半径が小さいため、よりしっかりと保持されます。
- サブシェルが安定しているため、電子を除去するには膨大なエネルギーが必要です。
2 番目のイオン化エンタルピーは、1 族の元素に比べて低くなります。それらは半分満たされた s サブシェルを持っており、より少ないエネルギーを使用して希ガスのオクテット構成を達成することで、電子を除去することが可能です。
水和エンタルピーは、原子半径に反比例します。グループのサイズが大きくなるにつれて、水和エンタルピーは減少します。
-
沸点と融点:
これらの元素は、サイズが小さく、結晶格子内でそれらの間の引力が強いため、アルカリ金属と比較して比較的高い融点と沸点を持っています。グループを下ると、マグネシウムが残り、沸点と融点が低下します。
-
アルカリ土類金属の陽性:
アルカリ土類金属は非常に陽性または金属的であり、グループを下るにつれて金属的特性が増加し続けます.イオン化エンタルピーが低いため、電子を失う傾向があり、容易に二価カチオンを形成して金属特性を高めます。
アルカリ土類金属は、アルカリ金属よりも低い金属特性を持っています。アルカリ金属よりもサイズが小さいため、原子核電荷が大きくなり、1 族元素よりも容易に電子を失う傾向が減少します。
-
絆の性質:
グループが下に行くにつれて、イオン結合を形成する傾向が増します。イオン化エンタルピーがグループの下に向かって減少するにつれて、イオン結合を形成する性質が増加します。イオン化エネルギーが減少するため、原子は電子を完全に失い、イオン結合を形成します。ベリリウムとマグネシウムはある種の共有結合を示しますが、他のすべての結合はイオン結合です。
-
密度:
これらの元素の密度は、グループの下でそのような傾向を示していませんが、サイズが小さく、それらの間の引力が強いため、グループ 1 の元素よりも密度が高くなっています。ただし、密度はベリリウムからカルシウムに減少し、カルシウムからバリウムに増加します。密度の低下は、結晶格子内の原子の充填効率の低下により説明できます。
-
火炎試験の着色:
グループ 1 の元素と同様に、アルカリ土類金属も特徴的な炎を示し、それを他の元素と区別します。これらの元素がより高いレベルに加熱されると、原子内の電子が励起され、より高い状態に移動します。基底状態に戻ると、吸収されたエネルギーは特定の波長の光の形で放出されます。
- カルシウムによる赤レンガ色
- ストロンチウムによる深紅色
- バリウムによるアップルグリーン色
- ラジウムによる真紅の色
サイズが小さいため、ベリリウムとマグネシウムは核に強く保持されているため、色を発しません。バーナーは、それらの電子が基底状態を離れるのに必要な熱を提供しません。したがって、彼らはそう簡単に電子を失うことはありません。
アルカリ土類金属の物理的性質の重要性
高い金属特性を示すアルカリ土類金属は、熱と電気の非常に優れた伝導体です。光沢がありますが、空気に触れるとすぐに変色します。ベリリウムでガラスを傷つけることは非常に困難です。逆に、バリウムは鉛よりも少し硬いです.
結論
アルカリ土類金属は、反応性の陽性または金属元素で、灰色がかった白の光沢のある光沢があります。これらは周期表の 2 番目のグループに属し、s サブシェルが満たされています。このグループの元素は、物理的および化学的にほぼ類似した特性を持っています。アルカリ土類金属の重要な物理的特性により、それらはさまざまな応用分野で非常に有用であることがわかっています。