ブロンステッド ローリー酸仮説は、デンマークの化学者ヨハネス ニコラウス ブロンステッドとトーマス マーティン ローリーによって 1923 年に最初に提案された酸塩基反応理論です。仮説によれば、酸と塩基は互いに相互作用し、酸は共役塩基を形成し、塩基もプロトン交換によって共役酸を形成します。ブロンステッド・ローリー仮説は、アレニウスの酸塩基理論のより高度な変種です。アレニウス仮説によると、酸は水溶液中の水素イオンの濃度を上昇させ、塩基は OH- イオンの割合を上昇させます。アレニウス理論には、水相中の酸と塩基の相互作用のみを検出するという制限があります。
ブレンステッド・ロウリー酸理論
仮説について
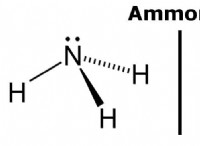
ブレンステッド・ローリー法によれば、成分はそのような塩基の存在下でのみ酸として作用するが、酸の非存在下では塩基としてのみ作用する.また、酸性物質はプロトンを1つ失うと酸共役塩基とも呼ばれる酸性溶液を作り、塩基性物質がプロトンを得ると塩基共役酸と呼ばれる酸を生成します。その結果、塩酸などの酸性化学物質とアンモニアなどの塩基性物質の反応は、次のように要約できます。
HCl +NH3⇌NH4++Cl-
アンモニウム イオン (NH4+) は確かに塩基性アンモニアの酸対応物であり、塩化物イオン (Cl-) は確かに上記の式に存在する塩酸の塩基対応物です。酸には、水酸化物イオン、アンモニウム イオン、およびさまざまな飽和金属陽イオンが含まれます。塩基には、リン、酢酸塩、硫化物、炭酸塩、およびハロゲン イオンが含まれます。
ブレンステッド ローリー酸
化学反応を通じて水素イオンを与える、または寄与する物質は、Bronsted-Lowry 酸として知られています。一方、ブレンステッド・ローリー塩基は水素イオンを吸収します。ブレンステッド・ロウリー酸はプロトンを提供しますが、塩基はプロトンを受け取ります。両性種とは、状況に応じて陽子を与えたり受け取ったりする種です。
各ブレンステッド ローリー酸は、そのプロトンを共役塩基分子に移動します。
HCl (aq) + NH3 (aq)→ NH4+ (aq) + Cl- (aq)
この次のプロセスの中で、塩酸 (HCl) はアンモニア (NH3) 上のプロトンに寄与し、アンモニウム カチオン (NH4+) と塩化物アニオン (Cl-) を形成します。塩化物イオンは確かに塩酸の共役塩基であり、Bronsted-Lowry 酸になります。
弱酸と強酸
水相では、強酸は成分イオンに完全に崩壊する物質です。強酸には、硝酸と硫酸があります。水とは、ヒドロニウムイオンと硝酸イオンに分離します。プロセス後の溶液には、溶解した HNO3 分子はありません。
一方、弱酸は、その成分イオンに完全には溶解しません。酢に含まれる酢酸は弱酸です。水と、酢酸は部分的にヒドロニウムと酢酸イオンに分離します。
ブレンステッド・ロウリー酸の重要性
<オール>結論
ブレンステッド・ローリー理論によると、酸と塩基はプロトン交換によって反応し、酸は共役塩基を生成し、塩基は共役酸を生成します。
ブレンステッド ローリー酸の重要性は、化学プロセス中に水素イオンを提供または供与することです。プロトンはブレンステッド・ローリー酸によって与えられ、塩基によって奪われます。両性種は、状況に応じて陽子を提供または受け入れることができる種です。