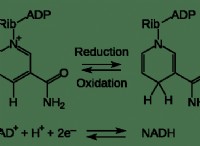
グループ1金属 :これらの要素は、周期表の左側にあり、アルカリ金属として知られています。それらは非常に反応性があり、単皮膜イオンを形成します。アルカリ金属は電気陰性度が低いため、電子を失う傾向が強いことを意味します。これにより、彼らは他の要素に対して最も外側の電子を容易に放棄するため、非常に反応性が高くなります。
比較 :
- 電気陰性度 :グループ17の元素は電気陰性度が高く、グループ1金属の電気陰性度は低いです。
- 反応性 :グループ17の元素は非常に反応性があり、珪藻分分子を形成しますが、グループ1要素は非常に反応性があり、単皮膜イオンを形成します。
- イオン化エネルギー :グループ17の要素はイオン化エネルギーが高く、グループ1要素のイオン化エネルギーは低いです。
- 融点と沸点 :グループ17の元素は融点と沸点が低く、グループ1の金属は融点と沸点が高くなります。
要約すると、グループ17の要素が強力な非金属であり、グループ1の金属が非常に反応性の金属である主な理由は、電気陰性度の違いによるものです。