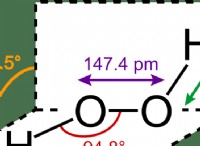
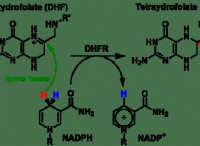
その理由は次のとおりです。
* 不平等な共有: 極性分子では、1つの原子が他の原子よりも強く共有電子を引き付けます。これは、より強い引力を持つ原子の電気陰性度が高いためです。
* 部分料金: より強いプルのある原子はわずかに負電荷(Δ-)を取得し、他の原子はわずかに正電荷(Δ+)を取得します。
* 双極子モーメント: この電荷の分離は、分子が正と負の終わりを持つ双極子モーメントを作成します。
例: 水(H₂O)は極分子です。酸素は水素よりも電気陰性度が高いため、共有電子をそれ自体に近づけます。これにより、酸素原子に部分的な負電荷が生じ、水素原子に部分的な正電荷が生成されます。
極性分子の他の例は次のとおりです。
* アンモニア(nh₃)
* 塩化水素(HCl)
* 二酸化炭素(CO₂)(線形構造にもかかわらず)
共有は極性分子では完全に等しくないにもかかわらず、電子はまだ *共有 *であり、共有結合であることを覚えておくことが重要です。不平等な共有は、単に分子内の電荷の分離につながります。