その理由は次のとおりです。
アルカリ金属との類似性:
* 電子構成: 水素は、アルカリ金属のように、最も外側の殻に1つの電子を持っています。
* 電子を失う傾向: 水素は、アルカリ金属と同様に、陽性イオン(H+)を形成するためにその唯一の電子を失う可能性があります。
* 非金属と反応: 水素は、ハロゲンのような非金属と反応して、非金属と反応するアルカリ金属と同様に、HClのような化合物を形成します。
ハロゲンとの類似性:
* 電子の獲得: 水素は、ハロゲンと同様に、電子を獲得して負イオン(H-)を形成できます。
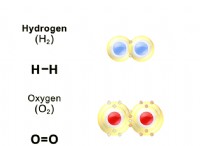
* 珪藻分子の形成: 水素は、ハロゲン(F2、Cl2、Br2、I2)と同様に、二原子分子(H2)として存在します。
* 金属と反応: 水素は、いくつかの金属と反応して、金属水素(NAH、CAH2など)を形成することができます。これは、金属と反応して塩を形成するハロゲンと同様です。
ただし、水素もユニークです:
* 小さなサイズと高い電気陰性度: 水素ははるかに小さく、アルカリ金属よりもはるかに高い電気陰性度を持っています。
* 金属格子を形成しません: アルカリの金属とは異なり、水素はその固体状態に金属格子を形成しません。
周期表への配置:
水素はグループ1のリチウムの上に配置されることがよくありますが、グループ17のフッ素の上に配置されることもあります。どちらのグループにも完全に収まらないため、独立したカテゴリに配置されることがよくあります。
最終的に、水素の配置は慣習の問題であり、アルカリ金属とハロゲンの両方でそのユニークな特性と類似性を理解することは役立ちます。