その理由は次のとおりです。
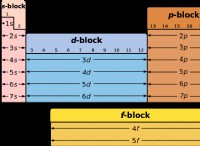
* 反応性: アルカリ金属(グループ1)およびアルカリ地球金属(グループ2)は、最も反応性のある金属です。これは、イオン化エネルギーが比較的低いことと、それぞれ陽性イオンを形成する1つまたは2つの電子を失う傾向があるためです。
* 遷移金属: 遷移金属は、周期表の中央ブロックを占めます。それらは、より複雑な電子構成を持ち、D軌道とS軌道の両方に電子を持つ、アルカリおよびアルカリ地球の金属よりも反応性が低い。 これにより、金属結合が強くなり、電子を失う傾向が低くなります。
遷移金属の例:
*鉄(fe)
*銅(CU)
*ゴールド(au)
*ニッケル(NI)
*プラチナ(PT)
遷移金属は一般に、アルカリおよびアルカリ地球金属よりも反応性が低いですが、例外があります。たとえば、マンガン(MN)のような一部の遷移金属は非常に反応性があります。