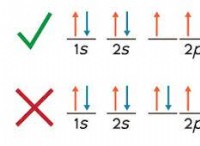
その理由は次のとおりです。
* 水の自己イオン化: 水(H2O)は、陽子(H+)を別の水分子に供与する傾向がわずかにあり、ハイドロニウムイオン(H3O+)と水酸化物イオン(OH-)を形成します。これは平衡によって表されます。
`` `
2 H2O <=> H3O + + OH-
`` `
* SO2の性質: 二酸化硫黄は共有化合物です。その結合は電子を共有することを伴い、水のようにイオンを容易に形成することはありません。 SO2は水と反応して硫酸(H2SO3)を形成することができますが、これは自己イオン化プロセスではなく、明確な化学反応です。
要約すると、SO2には水と同じ方法で自己イオン化しないため、SO2には「自己イオン化の産物」がありません。