* pHおよび濃度: pHは、溶液中の水素イオン(H+)濃度の尺度です。 H+濃度が高いほど、pHが低くなります(より酸性)。
* 希釈: 酸を希釈すると、溶液に溶媒(通常は水)を追加します。これにより、溶液中のH+イオンの濃度が減少します。
* pHへの影響: H+濃度は希釈時に減少するため、酸のpHは増加します(酸性が低くなります)。
例:
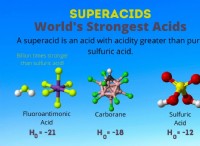
塩酸(HCL)のような強酸があると想像してください。 HClの濃縮溶液は非常に低いpH(高酸性)を持ちます。 この溶液に水を追加すると(希釈)、H+イオンがより広がり、濃度が減少します。 これにより、pHが高くなり、酸が酸性度が低いことを示します。
重要な注意: pHの変化は、希釈係数を使用して常に線形ではありません。 pHの特定の変化は、酸の初期濃度とその解離定数(KA)に依存します。