塩酸と酸化カルシウムの中和
塩酸(HCl)と酸化カルシウム(CAO)の間の反応は中和反応であり、塩化カルシウム(Cacl₂)と水(H₂O)を産生します。
反応方程式:
2 HCl(aq) + cao(s)→cacl₂(aq) +h₂o(l)
説明:
* 塩酸(HCl): 溶液中の水素イオン(H⁺)を容易に放出することを意味します。
* 酸化カルシウム(CAO): 基本的な酸化物は、水と反応して塩基(水酸化カルシウム、CA(OH)₂)を形成することを意味し、酸を中和します。
* 塩化カルシウム(Cacl₂): 酸とベースの反応から形成された塩。水に溶けます。
* 水(h₂o): 塩分からの水素イオンと塩基からの水酸化物イオンの組み合わせによって形成される反応の他の産物。
反応に関与するステップ:
1。酸化カルシウムは水と反応します: cao(s) +h₂o(l)→ca(oh)₂(aq)
2。水酸化カルシウムは塩酸を中和します: CA(OH)₂(AQ) + 2 HCl(aq)→CACL₂(aq) + 2H₂O(l)
全体:
この反応は発熱性であり、熱を放出します。この反応は、酸塩基反応の典型的な例でもあり、塩(hcl)が塩基(cao)によって中和され、塩(cacl₂)と水(h₂o)が形成されます。
アプリケーション:
この反応は、以下を含むさまざまなアプリケーションで一般的に使用されます。
* 産業プロセス: 酸性廃棄物の流れを中和する。
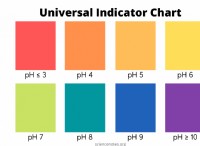
* 水処理: 水のpHを調整します。
* 構造: セメントとモルタルのコンポーネントとして。
安全上の注意事項:
* 塩酸は腐食性で有害です。 注意して処理し、適切な保護具を着用してください。
* 酸化カルシウムは水と激しく反応し、熱を発生させます。 取り扱いの際には注意してください。