hcl(aq) +h₂o(l)⇌h₃o⁺(aq) +cl⁻(aq)
方程式の各部分が表すものは次のとおりです。
* hcl(aq): 水に溶解した塩酸(水溶液)。
* h₂o(l): 液体水。
* h₃o⁺(aq): HClからのプロトン(H⁺)が水分子に付着すると形成されるヒドロニウムイオン。
* cl⁻(aq): 塩化物イオンは、HClがプロトンを失うと形成された負に帯電したイオンです。
キーポイント:
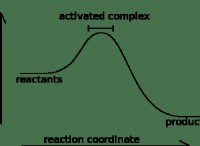
*反応は平衡反応です 、つまり、両方向に進みます。これは、二重矢印(⇌)で示されます。
* HClは強酸です 、つまり、それはほぼ完全に水中にイオン化することを意味します。 したがって、平衡は方程式の右側に大きく存在し、h₃o⁺イオンの形成を支持します。
*H₃o⁺イオンの存在は、塩酸酸を作るものです。