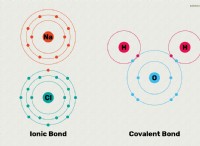
* 極性: 水は極性分子であり、つまり、わずかに正の端とわずかに負の端を持っています。塩(塩化ナトリウム、NaCl)は、陽性ナトリウムイオン(Na+)および陰性塩化物イオン(Cl-)を伴うイオン化合物です。水分子の正の末端は負の塩化物イオンを引き付け、水分子の負の端は正のナトリウムイオンを引き付けます。
* 水分補給: 水分子と塩イオンの間のこの魅力は、イオンの周りの水和シェルの形成につながります。水分子はイオンを効果的に囲み、隔離し、塩結晶にそれらをまとめるイオン結合を破壊します。
要するに、水は塩を溶解します:
1。誘引 塩のイオン。
2。周囲 水分子を備えたイオン。
3。バラバラに壊れます 塩水晶。
このプロセスは、塩が水に容易に溶解し、透明で塩辛い溶液を形成する理由です。