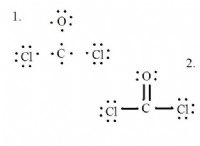1。分子形状と電子分布:
* 極結合: 異なる電気陰性度を持つ原子が結合すると、電子は不均一に共有され、極性結合が生じます。より電気陰性の原子が電子ペアを引き付けるほど、部分的な負電荷(Δ-)が得られ、電気陰性原子が少ない場合、部分的な正電荷(Δ+)が得られます。
* 分子形状: その分子形状と呼ばれる分子内の原子の3次元配置は、これらの極性結合がどのように配向されるかを決定します。
2。対称性と双極子モーメント:
* 対称分子: 極性結合が中心原子の周りに対称的に配置されている場合、個々の結合双極子(結合極性の方向と大きさを表すベクトル)が互いにキャンセルします。分子は非極性です 極性の結合がありますが。例:CO2、メタン(CH4)。
* 非対称分子: In asymmetrical molecules, the polar bonds are not evenly distributed, so the individual bond dipoles do not cancel out completely.これにより、ネットダイポールモーメントが作成されます 、分子極を作成します 。例:水(H2O)、アンモニア(NH3)。
3。例:
* 水(H2O): 酸素原子の孤立ペアのため、水は曲がっています。 2つのO-H結合は極性であり、曲がった形状により、双極子のモーメントがキャンセルされず、水が極分子になります。
* 二酸化炭素(CO2): CO2の線形形状は、2つの極性c =o結合を備えています。ただし、2つの双極子は反対方向を指し、互いにキャンセルしてCO2を非極性にします。
* メタン(CH4): メタンは、4つのC-H結合を備えた四面体の形状を持っています。これらの結合はわずかに極性ですが、四面体の形状により、個々の双極子がキャンセルし、非極性分子が発生します。
要約:
*極性分子は、電子密度の不均一な分布を持ち、その結果、正味の双極子モーメントが生じます。
*分子の形状は、個々の結合双極子がどのように相互作用するかを決定し、互いにキャンセルするか、正味の双極子モーメントを作成するかに影響を与えます。
*対称分子は非極性である傾向がありますが、非対称分子は通常極性です。
分子の形状と極性の関係を理解することは、溶解度、沸点、反応性など、分子の特性を予測するために不可欠です。