化学結合による
* イオン化合物: 反対に帯電したイオン間の静電引力によって形成されます。それらは通常、金属と非金属を伴います。例:NaCl(テーブルソルト)、MGCL2(塩化マグネシウム)。
* 共有化合物: 原子間の電子の共有によって形成されます。それらは通常、非金属を伴います。例:H2O(水)、CO2(二酸化炭素)。
* 金属化合物: 「電子の海」の金属原子間の電子の共有によって形成されます。例:金(AU)、銅(CU)。
要素の数による
* バイナリ化合物: 2つの異なる要素で構成されています。例:H2O、NaCl。
* 三元化合物: 3つの異なる要素で構成されています。例:H2SO4(硫酸)、NAHCO3(重炭酸ナトリウム)。
* 四級化合物: 4つの異なる要素で構成されています。 例:CH3COOH(酢酸)。
関数群による:
* 炭化水素: 炭素と水素のみを含む化合物。例:メタン(CH4)、エタン(C2H6)。
* アルコール: ヒドロキシル(-OH)グループが含まれています。例:エタノール(C2H5OH)、メタノール(CH3OH)。
* aldehydes: 炭素鎖の終わりにカルボニル基(-CHO)を含む。例:ホルムアルデヒド(HCHO)、アセトアルデヒド(CH3CHO)。
* ケトン: 炭素鎖内にカルボニル基(-CO-)が含まれています。例:アセトン(CH3COCH3)、プロパノン(CH3COCH2CH3)。
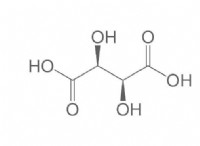
* カルボン酸: カルボキシル基(-COOH)が含まれています。例:酢酸(CH3COOH)、ギ酸(HCOOH)。
* アミン: アミノ基(-NH2)が含まれています。例:メチルアミン(CH3NH2)、エチルアミン(CH3CH2NH2)。
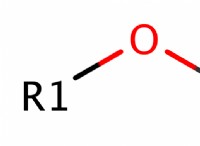
* エーテル: 2つのカーボンチェーンを接続するエーテル基(-O-)が含まれています。例:ジエチルエーテル(CH3CH2OCH2CH3)、ジメチルエーテル(CH3OCH3)。
物理状態:
* ソリッド: 固定された形状とボリュームがあります。例:NaCl、ICE。
* 液体: 固定ボリュームを持っていますが、容器の形をとってください。例:水、水銀。
* ガス: 固定された形やボリュームはありません。例:酸素、窒素。
他の分類による:
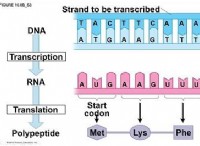
* 有機化合物: 通常、水素、酸素、窒素、およびその他の元素と結合した炭素原子が含まれています。例:グルコース(C6H12O6)、タンパク質、DNA。
* 無機化合物: 炭素原子は含まれていません(炭酸塩やシアン化物などのいくつかの例外を除く)。例:NaCl、H2O、CO2。
これは単なる基本的な概要であり、化合物のより詳細な分類がたくさんあります。 たとえば、有機化学内では、原子と官能基の特定の配置に基づいたさらに分類があります。 化合物を分類する方法は、コンテキストと、理解する最も重要な側面に依存します。