* 彼らは陽子を寄付します: これは、Brønsted-Lowry酸の決定的な特徴です。それらは、水素イオン(H+)を容易に放出します。
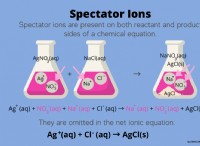
* 共役塩基:を形成できます 酸がプロトンを寄付すると、共役ベースを形成します。コンジュゲートベースは、陽子が除去された後に残っている種です。たとえば、HClがプロトンを寄付すると、Cl-を形成します。これは、その共役ベースです。
* 溶液中のH+イオンの濃度を増加させる: 酸が水に溶けると、H+イオンが放出され、溶液の酸性度が高まります。
* 例: HCl(塩酸)、H2SO4(硫酸)、HNO3(硝酸)、Ch3COOH(酢酸)、およびNH4+(アンモニウムイオン)。
覚えておくべきキーポイント:
*Brønsted-Lowryの定義は、酸のArrheniusの定義(水中でH+イオンを産生する物質にのみ適用される)よりも広いです。
*陽子を寄付するすべての物質は、Brønsted-Lowryの意味での酸ではありません。たとえば、水は酸とベースの両方として機能します。
これ以上質問がある場合はお知らせください!