ルイス酸と塩基
* ルイス酸: 電子ペアを受け入れる物質。
* ルイスベース: 電子ペアを寄付する物質。
水酸化物の場合(OH-)
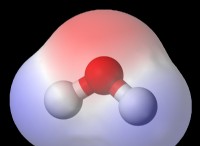
1。孤立ペア: 水酸化物(OH-)の酸素原子には、電子の2つのペアがあります。
2。寄付: これらの唯一のペアは、電子不足種(ルイス酸)に寄付できるように容易に利用できます。
例:水酸化物とプロトン(H+)との反応
* h+(陽子): プロトンは、電子ペアがなく、それを求めるため、ルイス酸です。
* oh-(水酸化物): 水酸化物には2つの孤立ペアがあり、ルイスベースになります。
* 反応: プロトン(H+)が水酸化物(OH-)と反応すると、水酸化物の酸素原子の孤立ペアがプロトンとの新しい結合を形成し、水(H2O)を生成します。
H + + OH-→H2O
結論
水酸化物は、電子不足種(ルイス酸)に寄付できる電子の容易なペアを容易に利用できるため、ルイスベースです。新しい結合を形成します。