1。塩水:
* 電解質: 海水には、電解質として機能する溶存塩が含まれており、電流の流れが可能です。これにより、腐食を促進する電気化学反応が促進されます。
* 塩化物: 塩化物イオン(CL-)は特に攻撃的で容易に金属表面を容易に攻撃し、しばしば溶けになり、金属構造を弱める金属塩化物を形成します。
2。酸素:
* 溶解酸素: 海水には溶存酸素が含まれており、腐食プロセスで酸化剤として機能します。酸素は金属と反応し、金属をさらに劣化させる金属酸化物(錆)を形成します。
3。湿度:
* 高湿度: 海の近くの高い湿度は、腐食を促進する湿った環境を提供します。水分子は金属表面に薄膜を形成し、腐食に関与する化学反応を促進します。
4。摩耗:
* 波動アクション: 波と強い電流は摩耗を引き起こす可能性があり、それが保護コーティングを除去し、金属を腐食性環境にさらします。
5。海洋生物:
* バイオフーリング: フジツボ、藻類、海藻などの海洋生物は、金属表面に付着することができます。これらの生物は、水分を捕まえて腐食を促進する微小環境を作り出します。
6。温度変動:
* 温度変動: 沿岸地域の変動温度は、腐食プロセスを加速します。
7。汚染物質:
* 産業汚染: 産業活動は汚染物質を海に放出し、腐食性の環境をさらに強化することができます。
腐食がどのように起こるか:
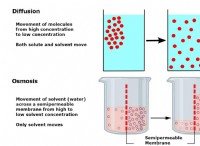
塩味の環境での腐食は、通常、電気化学プロセスを通じて発生します。
* アノード: 金属表面は、酸化が発生するアノードとして機能します(電子の喪失)。
* カソード: 金属表面の別の領域または別の材料(破片など)は、還元が発生するカソードとして機能します(電子の獲得)。
* 電解質: 塩水は電解質として機能し、アノードとカソード間の電子の流れを可能にします。
最終的な結果は、金属表面上の腐食生成物の形成と金属の弱体化です。
例:
*酸化鉄(錆)の形成により、鉄(鋼)は海の近くで急速に錆びます。
*塩水で銅が腐食し、緑の緑青(炭酸銅)を形成します。
*海水でアルミニウムは腐食しますが、さらに腐食を遅くする保護酸化物層を形成します。
要約すると、塩水、酸素、湿度、摩耗、海洋生物、温度変動、および汚染物質の組み合わせは、海の近くの金属に非常に腐食性の環境を作り出します。