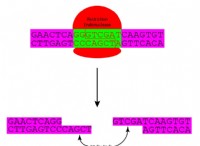
何が起こるか:
* 原子の再配置: 化学反応には、原子間の化学結合の破壊と形成が含まれます。これにより、分子内の原子の配置が変化し、新しい物質が形成されます。
* エネルギーの変化: 反応は、エネルギー(発熱)を放出するか、エネルギー入力(吸熱)を必要とする可能性があります。エネルギーの変化の量は、反応の自発性と、どのくらいの熱が生成または吸収されるかについて説明できます。
* 新しい物質の形成: 出発材料(反応物)は、異なる物質(製品)に変換されます。化学式と特性によって製品を識別できます。
それがどのように機能するか:
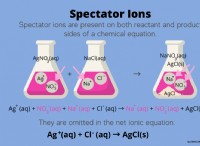
* 反応方程式: 化学式は、反応の象徴的な表現を提供します。反応物と生成物の化学式、および化学量論(各物質の相対量)を示します。
* 反応条件: 反応が起こる条件(温度、圧力、触媒)は、反応の速度と方向に影響を与える可能性があります。
* 反応動態: 化学の分岐は、化学反応の速度とメカニズムを研究し、反応がどれだけ速く進行し、段階が関係するかを明らかにします。
それがあなたに伝えることができること:
* 製品の識別: 反応物と反応条件を知ることで、形成された製品を予測できます。
* 反応の実現可能性の予測: 熱力学は、特定の条件下で反応が自発的に発生するかどうかを判断するのに役立ちます。
* 反応結果の制御: 反応条件と速度論を理解することにより、反応を操作して望ましい製品を生産することができます。
* 私たちの周りの世界を理解する: 化学反応は、光合成から燃焼、岩や鉱物の形成まで、自然界で無数のプロセスを促進します。
例:
* 燃焼: 燃える木材はエネルギー(発熱)を放出し、木材を灰、二酸化炭素、水に変換します。
* 光合成: 植物は日光エネルギー(吸熱)を使用して、二酸化炭素と水をグルコースと酸素に変換します。
* 錆び: 鉄は酸素と水と反応して、酸化鉄(錆)を形成します。これは、金属を悪化させるプロセスです。
化学反応を研究することにより、物質の基本的な構成要素とそれらがどのように相互作用するかについての洞察を得て、私たちの周りの世界のより深い理解につながります。