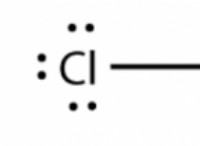控えめに溶けやすい塩についての重要なポイントの内訳は次のとおりです。
特性:
* 溶解度が低い: それらの溶解度製品定数(ksp)は小さいです。 KSPは、固体イオン化合物が水に溶解する程度を表す平衡定数です。
* 限られた範囲で溶解: 控えめに可溶性の塩を水に加えると、溶液中の解散固体とそのイオンの間に平衡が確立されます。この平衡は左にあります。つまり、ほとんどの塩は溶解していないことを意味します。
* 降水反応: 控えめに溶けやすい塩は、多くの場合、沈殿反応に関与します。そこでは、成分イオンが溶液中に出会うと固体沈殿物が形成されます。
例:
* 塩化銀(AGCL): 写真で使用され、銀イオンの分析に使用されます。
* 炭酸カルシウム(CACO3): 石灰岩、大理石、貝殻の主要成分。
* 塩化鉛(PBCL2): 鉛蓄電池の製造に使用されます。
* 硫酸バリウム(BASO4): X線の造影剤として使用されます。
溶解度に影響する要因:
* 温度: 一般に溶解度は温度とともに増加しますが、これは常に溶けやすい塩の場合ではありません。
* 一般的なイオン効果: 一般的なイオン(溶液中にすでに存在するイオン)の存在は、控えめに可溶性の塩の溶解度を低下させる可能性があります。
* ph: 溶液のpHは、一部の塩の溶解度に影響を与える可能性があります。
アプリケーション:
* 分析化学: 控えめに溶けやすい塩は、沈殿物の質量を使用してサンプル内の物質の量を決定するために使用されます。
* 環境科学: 控えめに溶けやすい塩の溶解度は、環境での汚染物質の水質と輸送に役割を果たします。
* 薬: いくつかの控えめな溶けやすい塩は、たとえば制酸剤として炭酸カルシウムなど、薬物として使用されます。
全体として、特に化学、環境科学、医学において、さまざまな科学的および実用的な用途にとって、控えめに溶けやすい塩の挙動を理解することが重要です。