その理由は次のとおりです。
* 電子構成: 炭素には6つの電子があり、構成1S²2S²2p²があります。これは、外側のシェル(2番目のシェル)に4つの電子があることを意味します。
* 価電子: これらの4つの電子は原子価電子と呼ばれ、化学的結合に関与する電子と呼ばれます。
* オクテットルール: 炭素は、オクテットのルールに従う傾向があります。つまり、安定性のために外側のシェルに8つの電子を持ちたいと考えています。
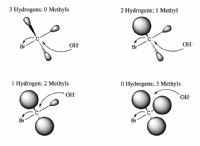
* Tetravalence: オクテットを達成するには、炭素はさらに4つの電子を獲得または共有する必要があります。これが、4つの結合を形成し、四面系になっている理由です。
簡単に言えば: 炭素は外側のシェルに4つの「空のスロット」を持っているため、他の原子と4つの結合を形成して、それらのスロットを埋めて安定になります。これがその四量体の本質です。