その理由は次のとおりです。
* 価電子 原子の最も外側のエネルギーレベルの電子です。彼らは核から最も遠いものであり、それに対する最も弱い魅力を経験します。
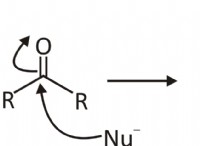
* 化学結合 原子間の電子の共有または伝達を伴います。 価電子は、他の原子と相互作用するために容易に利用できるものです。
* 内側のシェル電子 (エネルギーレベルが低い電子)は、核にしっかりと結合しており、結合に簡単に関与していません。
例:
*酸素には8つの電子があります。最初のシェルに2つ、2番目のシェルに6つの電子があります。 2番目のシェルの6つの電子は、原子価電子です。
*酸素は、その原子価電子を水(H₂O)などの他の原子と共有することにより、結合を形成します。
キーテイクアウト: 原子価の電子は、原子の化学的挙動と他の原子と結合を形成する能力を決定します。