その理由は次のとおりです。
* 中和: 酸塩基反応の決定的な特徴は、酸と塩基が反応して塩と水を形成し、互いの特性を効果的に中和することです。
* 二重変位: 二重変位反応では、2つの反応物の正と陰性のイオンが場所を切り替えます。 酸塩基反応の場合、酸からの水素イオン(H+)は、塩基から水酸化物イオン(OH-)と結合して水(H2O)(H2O)を組み合わせています。残りのイオンは塩を形成します。
例:
塩酸(HCL)と水酸化ナトリウム(NAOH)との反応は、古典的な例です。
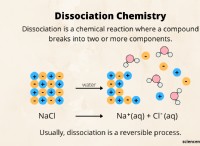
HCl(酸) + NaOH(ベース)→NaCl(塩) + H2O(水)
H+とOh-イオンがどのように結合され、残りのNa+およびCl-イオンが塩化ナトリウム(NaCl)を形成するかを見ることができます。