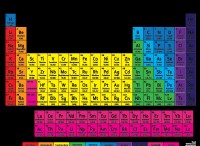
sおよびpブロック要素:
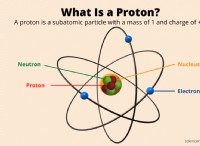
* 価電子: これらの要素には、SおよびP軌道に価電子電子があります。
* 単純なイオン化パターン: 安定した高貴なガス構成を実現するために、予測可能な数の電子を失うか、獲得する傾向があります。たとえば、アルカリ金属(グループ1)は1つの電子を失い、+1になり、ハロゲン(グループ17)は1つの電子を獲得して-1になります。
dブロック要素(遷移金属):
* 多価電子電子: それらは、D軌道とS軌道の両方に価電子を持っています。
* 可変イオン化パターン: 結合にD電子とS電子の両方が関与しているため、これらの要素は異なる組み合わせで電子を失ったり獲得したりする可能性があります。
* d軌道の影響: D軌道は、内側のD軌道と比較して、結合のためによりエネルギー的にアクセスしやすく、酸化状態の柔軟性を高めることができます。
例:
* s-block: ナトリウム(NA)の酸化数は+1です。
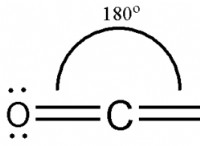
* pブロック: 酸素(O)の酸化数は-2です。
* d-block: 鉄(Fe)には、Feo(酸化鉄)およびFe₂o(鉄(III)酸化物)に見られるように、酸化数は+2と+3の酸化数を持つことができます。
例外:
この一般化には例外があることに注意することが重要です。一部のSブロックおよびPブロック要素には、複数の酸化状態、特にスズ(SN)や鉛(PB)などの重い要素があります。
これ以上質問がある場合はお知らせください!