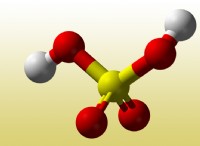
その理由は次のとおりです。
* 価電子: 酸素(O)には6つの原子価電子があり、窒素(N)には5、塩素(Cl)には7つあり、シンボル「L」の要素はありません。 安定した分子を形成するには、原子が完全な外側シェル(通常8電子)を達成するために電子を共有または伝達する必要があります。
* 結合ルール: これらの要素の組み合わせは、典型的な結合ルールに従いません。 酸素と窒素は複数の結合を形成できますが、塩素は通常1つの結合のみを形成します。
誤解の可能性:
別の式を書くつもりだった可能性があります。いくつかの可能性には以下が含まれます:
* nocl(塩化ニトロシル): この分子は存在し、中心に窒素原子を含む線形構造を持っています。
* oncl(塩化ニトリル): この分子も存在し、中心に窒素原子を含む平面構造を持っています。
特定の構造を提供するには、意図した式を明確にする必要があります。