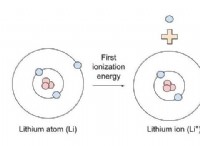
* 電子: 電子は、原子の核を周回する負に帯電した粒子です。
* 価電子: これらは、原子の最も外側の殻の電子であり、化学結合に関与する電子です。
* 配置と番号:
* 番号: 価電子の数は、原子の結合容量を決定します。たとえば、1つの原子価電子を持つ元素はそれを失う傾向がありますが、7つの価電子を持つ要素は1つを獲得する傾向があります。
* アレンジメント: これらの電子の特定の配置は、軌道(電子が見つかる可能性が高い空間の領域)における原子の反応性と、形成できる結合の種類に影響します。
これらの要因が化学的性質にどのように影響するかは次のとおりです。
* 反応性: より容易に利用可能な原子価電子(1つの原子価電子を持つアルカリ金属など)を備えた元素は非常に反応性があります。完全な価数貝殻(貴族のような)を備えた要素は非常に反応しません。
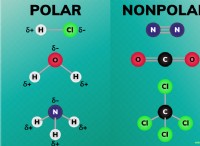
* 結合: 原子価電子の数と配置は、要素が形成できる結合のタイプを決定します。
*電子電子がほとんどない元素は、電子を失うことによりイオン結合を形成する傾向があります。
*多くの価電子を持つ元素は、電子を共有することにより共有結合を形成する傾向があります。
* 酸化状態: 化学反応中に原子が電子を獲得または失う傾向は、その酸化状態に反映されます。これは、価電子の数に直接関連しています。
要約: 原子の最も外側のシェル内の価電子電子の配置と数は、反応性、結合挙動、酸化状態など、化学的特性を決定する重要な要因です。