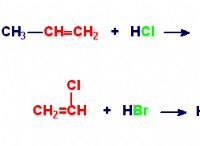
これが故障です:
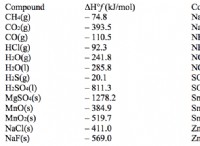
* エンタルピー システムの総熱含有量を表す熱力学的特性です。
* エンタルピー変化(ΔH) 化学反応の生成物と反応物間のエンタルピーの違いです。
* 発熱反応 周囲にエネルギーを放出し、負のエンタルピー変化をもたらします(ΔH<0)。
* 吸熱反応 周囲からエネルギーを吸収し、その結果、正のエンタルピー変化をもたらします(ΔH> 0)。
したがって、化合物が反応してエネルギーを放出すると、それは製品の反応物よりもエンタルピーが低いためです。エンタルピーの違いは、熱、光、または他の形態のエネルギーとして放出されるエネルギーです。