ニッケルには銀白色の色合いがあります。硬く、可鍛性があり、延性がある金属。鉄のグループに属し、磨き上げることで高い輝きを放ちます。このため、熱と電気の両方の適度に優れた伝導体です。ニッケルは、他の原子価を取ることができるという事実にもかかわらず、よく知られている化合物では二価です。また、さまざまな複雑な化合物を形成する能力もあります。ニッケル化合物の大部分は青色または緑色です。ニッケルは希酸にゆっくりと溶解しますが、硝酸で処理すると、鉄と同様に不活性になります。細かく砕いたニッケルは水素を吸着します。
特徴
<オール> ニッケルは、他の金属を保護するためにメッキするために使用される耐腐食性金属です。一方、主にステンレス鋼などの合金の製造に使用されます。ニクロムは主にニッケルとクロムで構成された合金で、微量のケイ素、マンガン、鉄が適切な量で投入されています。
非常に高温でも耐食性があるため、トースターや電気オーブンで使用されています。
海水を淡水に変換する淡水化プラントでは、構造の一部として銅ニッケル合金がよく使用されます。ニッケル鋼は装甲車両のメッキに使用されています。
その他のニッケル合金は、ボートのプロペラ シャフトやタービン ブレードの製造に使用されています。
ハイブリッド車に使用される充電式ニッケルカドミウム電池やニッケル水素電池などの電池には、ニッケルが広く使用されています。ニッケルは、古くから貨幣に使用されてきた長い歴史があります。
細かく分割されたニッケルは、植物油の水素化の触媒として使用されます。ガラスにニッケルを添加すると緑色になります。ニッケルは銅の 2 倍の量があり、地球の地殻の約 0.007% を占めています。火成岩の非常に一般的な成分ですが、濃度、サイズ、入手しやすさの点で商業的関心の基準を満たす鉱床はごくわずかです。
地球の中央部にはかなりの量のウランが含まれていると考えられています。ニッケルの最も重要な供給源のいくつかはペントランダイトであり、ニッケルを含む磁硫鉄鉱 (3 ~ 5% のニッケルを含むものもある) と黄銅鉱、およびマグネシウムであるガーニエライトなどのニッケルを含むラテライトで見つけることができます。 –可変組成および組成のケイ酸ニッケル
ニッケルの化学的性質
グループ 10
融点 1455°C、2651°F、1728 K
ピリオド 4
沸点 2913°C、5275°F、3186 K
ブロック d
密度 (グラム/立方センチメートル)
8.90
周期表の数字 28
原子質量は、宇宙の他の部分と比較して 58.693 g です。
温度を 20°C に保ちます。
しっかりしたキーを持つ同位体
[Ar] 3d84s2 58Ni 電子配置 [58Ni]
7440-02-0 は、この化合物の CAS 番号です。
ChemSpider ID 番号 910
ChemSpider は、無料で利用できる化学構造データベースです。
ニッケルにはさまざまな用途があります
<オール> おそらく、この要素の最も重要な用途は硬貨の製造です。
ワイヤーの製造に利用されています。
ガスタービンやロケット エンジンで使用される場合、高温にさらされても腐食に耐えることができるため、選択されます。
さまざまな合金の作成に使用され、その後、装甲板、釘、パイプなどの製造に利用されます。
モネル (ニッケルと銅の合金) は、海水やその他の化学物質による腐食に耐えることができる硬い物質です。その結果、ボートや海水淡水化プラントのプロペラ シャフトなどに使用されています。
ニッケルの物理的特徴
<オール> ニッケルは銀白色で硬く、可鍛性と延性に優れた金属です。
熱と電気の良導体であり、軽量でもあります。
それは 2 価です。つまり、他の元素とは対照的に、2 の原子価を持つことを意味します。
希酸にさらされると、金属はゆっくりと溶解します。
融点は摂氏 1453 度、沸点は摂氏 2913 度です。
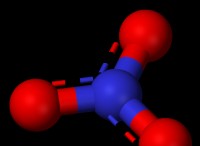
[NiCl4]2 形状 [NiCl4]2
Ni2+ は sp3 ハイブリダイゼーションを起こし、その結果、四面体配置の Cl– 配位子との結合が形成されます。 d 軌道には不対電子があるため、[NiCl4]2 は常磁性であり、不対電子のスピン数が高いため、高スピン外部軌道複合体と呼ばれます。その結果、[NiCl4]2 分子は四面体になります。
結論
したがって、それは放射性金属であるため、有毒であり、人間の健康に危険であると結論付けることができます. 99Tc は、本質的に非常に汚染性が高く、人間の健康に危険な化学物質です。化学薬品を扱うときは、保護手袋を着用する必要があります。