化学では、化学結合は、原子やイオンなどのさまざまな構成要素を結合し、全体のエネルギーを失うことによってそれらを安定化させる引力です。したがって、化合物の強度が形成される結合に依存することは明らかです。また、化学結合は安定性に比例します。つまり、化合物間の結合が強いほど、その分子の安定性が高くなります。一方、分子構造は膨大な議論であるため、この記事では構造の種類とその基本的な説明について説明します。
絆に関連する理論
<オール>ルイス理論
1916 年、ギルバート ルイスは希ガスの不活性に基づいて化学結合の形成を説明することに成功しました。この理論によると、原子は犬小屋 (正電荷) と外殻で構成されています。電子は外殻を占め、この犬小屋を取り囲んでいます。したがって、8個の電子を持つ原子は安定した配置になります。これは、最も外側のシェルが完全に占有されている場合、原子が安定した結合を形成することを意味します。また、価電子 (最外殻に存在する電子) のみが化学結合の形成に関与します。
<オール>コッセルの理論
希ガスは、電気陽性度の高いアルカリ金属と電気陰性度の高いアルカリ土類金属を分離する傾向があります。これらのハロゲンは負に帯電したイオンを形成する傾向があり、貴金属は正に帯電したアルカリ金属を形成します。これらの負および正に帯電したイオンは、8 個の電子を持つ安定した構成を持ち、ns2np6 によって与えられます。これらの反対に荷電された粒子は、静電引力により結合が形成され、この結合は電子結合と呼ばれます。
債券の種類
反応に応じて、反応中に形成される結合の種類を予測できます
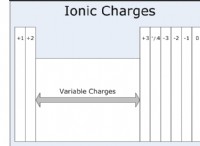
<オール>イオン結合
電子の移動によって形成される結合は、イオン結合と呼ばれます。ここで、一方の原子は電子を失い、陽イオンとも呼ばれる正に帯電した原子になりますが、電子を獲得したもう一方の原子は負になり、陰イオンと呼ばれます。陽イオンと陰イオンの間の電荷の不均衡が大きいほど、結合は強くなります。
<オール>共有結合
2つの原子間で電子を共有することによって形成される結合は、共有結合と呼ばれます。炭素を含む化合物は、主に共有結合を形成します。
<オール>極性結合
結合を形成する2つの原子間の電子分布が不均一な場合、極性結合が形成されます。共有結合とイオン結合の間の境界線は極性結合です。通常、電気陰性度の差が 0.4 未満の原子は、非極性の共有結合と見なされます。
<オール>金属結合
電子雲がイオン中心の周りに形成されると、形成される結合は金属結合と呼ばれます。共有結合やイオン結合と比較して、金属結合は電気伝導性と熱伝導性が高いです。
分子構造は膨大な議論ですが、現在の記事では、構造の種類とその基本的な説明について説明します。
分子構造
孤立電子対と結合対を組み合わせて予測された理想的な分子構造に応じて、いくつかの構造を以下に示します。上記の構造を区別する最も一般的な要因は結合角です。これは、分子内の 2 つの隣接する結合の間の角度に他なりません。
<オール>結論:
構造と幾何学についてもっと知るには、価電子殻電子対反発理論を読んで理解することができます。いいえとして。分子内の電子の変化は、その全体的な構造が変換されます。これは、化学構造が電子変換により変更され、異なる形状につながることを証明しています。一方、異なる化学結合は、ルイスの理論と核理論という2つの異なる理論に関連付けられています。これらの理論を理解すると、分子内に存在する化学結合が極性、イオン性、共有結合、金属のいずれであるかを予測するのが容易になります。これらの結合には、化学者が簡単に区別できるさまざまな特性があります。この記事では、さまざまな原子の化学結合と結合構造、それらの基本的な違い、結合角度、および構造がどのように形成されるかについて説明しました.