その理由は次のとおりです。
* 両性酸化物 酸と塩基の両方として作用できます。
* 酸を含む 、彼らは塩基として機能し、塩と水を形成するために陽子(H+)を受け入れます。
* ベース 、彼らは酸として作用し、塩と水を形成するために陽子(H+)を寄付します。
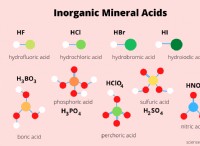
両性酸化物の例:
* 酸化アルミニウム(al₂o₃)
* 酸化亜鉛(ZnO)
* 鉛(II)酸化物(PBO)
* スズ(II)酸化物(SNO)
反応:
塩酸を伴う:
*al₂o₃ + 6hcl→2alcl₃ +3h₂o
* ZnO + 2HCl→Zncl₂ +H₂o
水酸化ナトリウム:
*al₂o₃ + 2naoh +3h₂o→2na [al(oh)₄]
* ZnO + 2NAOH +H₂O→Na₂[Zn(OH)₄]
重要な注意: 遷移金属のものと同様に、一部の酸化物は、酸化状態と反応条件に応じて両性挙動を示す可能性があります。