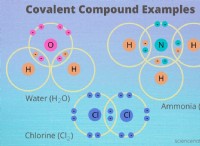
その理由は次のとおりです。
* 結合: 非金属は通常、共有結合を形成します。これは、金属に見られる金属結合よりも弱いです。 共有結合には電子の共有が含まれますが、金属結合には非局在電子の「海」が含まれます。
* 分子間力: 非金属は、しばしば液体状態でそれらをまとめる(ファンデルワールスの力など)より弱い分子間力を持っています。これらの力は、金属の金属結合よりも弱いです。
例外:
この一般的なルールにはいくつかの例外があります。
* ネットワーク共有固体: 炭素(ダイヤモンドの形)や二酸化シリコン(SIO2、石英)などの一部の非金属は、強力なネットワーク共有構造のため、非常に高い沸点を持っています。
* 珪藻類の非金属: 窒素(N2)や酸素(O2)のような珪藻類の非金属は、弱いファンデルワールスの力によって一緒に保持されるため、沸点が比較的低くなっています。
要約: 例外もありますが、一般に、非金属は、結合と分子間の力が弱いため、金属よりも沸点が低い傾向があります。