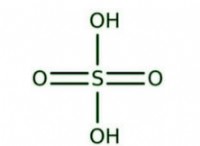
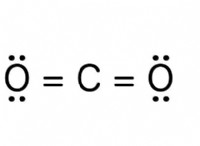その理由は次のとおりです。
* 酸 水素イオン(H+)を溶液に寄付します。
* ベース 溶液から水素イオン(H+)を受け入れます。
このプロセスはプロトン化と呼ばれます 。 塩基が水素イオンを受け入れると、プロトン化されます。
ベースにはさまざまな種類があります。
* arrheniusベース 溶液中に水酸化物イオン(OH-)を生成し、水素イオンと反応して水を形成します。
* brønsted-lowryベース 陽子(H+)を受け入れることができる物質です。
* ルイスベース 電子ペアのドナーであり、水素イオンとその電子ペアを共有することにより、プロトンを受け入れることができます。
ベースの例:
* 水酸化ナトリウム(NaOH) 水酸化物イオンを容易に寄付する強力なアレニウスベースです。
* アンモニア(NH3) は、アンモニウムイオン(NH4+)を形成するためにプロトンを受け入れることができるBRønSted-Lowryベースです。
* 炭酸イオン(Co3^2-) プロトンを受け入れるために電子ペアを寄付できるルイスベースです。
特定の種類のベースに関する詳細情報をご希望の場合はお知らせください!