1。 Cu²⁺イオンの還元:
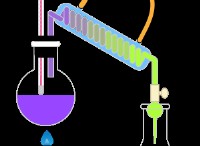
* カソードで: 銅イオン(Cu²⁺)は、電子を獲得することにより銅金属(Cu)に還元されます。この反応は、溶液からcu²⁺イオンを除去し、銅イオンの濃度を減少させます。
* 方程式: cu²⁺(aq) +2e⁻→cu(s)
2。塩化物イオンの形成:
* アノードで: 塩化物イオン(Cl⁻)は、電子を失うことにより塩素ガス(Cl₂)に酸化されます。この反応は、溶液中の塩化物イオンの濃度を増加させます。
* 方程式: 2cl⁻(aq)→cl₂(g) +2e⁻
3。色の変化:
*塩化銅溶液の青い色は、水和銅イオン(Cu²⁺(aq))の存在によるものです。
*電解中にcu²⁺イオンの濃度が減少すると、青色の強度がフェードされます。
*さらに、塩素ガスの形成は、水と反応して色気のない血色の良い酸(HOCL)を形成することができるため、青色の衰退にも寄与する可能性があります。
全体として、塩化銅の電気分解中の青色の衰退は、cu²⁺イオンの枯渇とclotionsの形成によるものです。電気分解が進むにつれて、ソリューションは次第に青くなりません。
注: 色の変化は、カソードに銅の金属堆積の直接的な結果ではありません。銅の金属は赤みがかった茶色ですが、溶液は赤茶色ではなく、軽い青または無色にフェードします。