* 対称性は、個々の結合ではなく、分子の形状に焦点を当てています。 対称分子には、中心点の反対側に同一の部分があります。 この対称性は、分子 *内で電子密度を均等に分布させることができ、全体的に非極性になります。
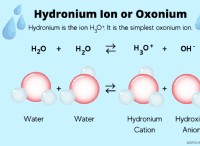
* 結合極性は、電気陰性度の違いに依存します。 有意に異なる電気陰性度の値を持つ2つの原子が電子を共有すると、極性結合が形成されます。これにより、電気陰性度の低い原子に部分的な正電荷が生成され、より多くの電気陰性原子に部分的な負電荷が生成されます。
例を示します:
* 二酸化炭素(CO2) 対称形状の線形分子です。ただし、酸素原子は炭素原子よりも電気陰性です。これにより、極C =O結合が作成されます。 分子は対称的ですが、線形配置のために極性結合は完全にはキャンセルされません。 したがって、CO2は極性分子と見なされます。
概要:
* 対称性は、すべての結合が非極性である場合、または極性結合が互いにキャンセルする場合、非極性分子につながる可能性があります。
* 原子が有意に異なる電気陰性度値を持っている場合、対称的な分子は依然として極性結合を持つことがあります。